Основания представляют собой вещества, способные принять протон (H+) и образовать соль и воду. Как известно, протоны являются положительно заряженными частицами, поэтому основания могут реагировать с другими основаниями. Данная особенность оснований имеет свои особенности и может проявляться в различных химических реакциях.
Реакции между основаниями могут протекать различными способами. Одним из наиболее известных типов реакций является реакция нейтрализации. В такой реакции основание реагирует с кислотой, образуя соль и воду. Например, реакция между гидроксидом натрия (NaOH) и гидроксидом калия (KOH) может происходить следующим образом:
2 NaOH + KOH → Na2K(OH)2
В данном случае оба основания реагируют между собой, образуя новое основание с элементами обоих исходных веществ.
Реакции между основаниями также могут быть полезными в промышленности и научных исследованиях. Например, при производстве мыла происходит реакция между щелочным (NaOH) и жирными кислотами. Эта реакция позволяет получить мыло и глицерин. Также, реакции между различными основаниями могут быть использованы для получения различных солей и соединений при производстве химических веществ.
Химические реакции между основаниями
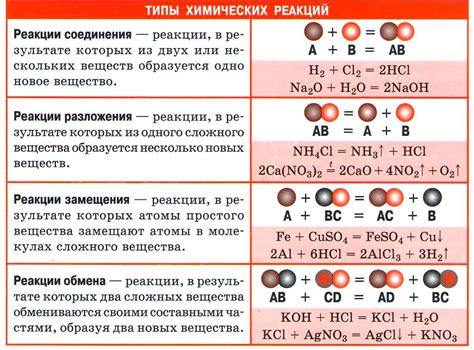
Когда два основания встречаются в растворе, они могут образовывать новые соединения или происходить просто нейтрализация. Если соединение, образованное из двух оснований, кроме соли и воды, сохраняет свойства основания, то такую реакцию называют амфотерной.
Примером амфотерной реакции между одними основаниями может служить взаимодействие гидроксида алюминия (Al(OH)3) и гидроксида железа(III) (Fe(OH)3).
Al(OH)3 + Fe(OH)3 → Al(OH)4- + Fe(OH)2+
В результате этой реакции образуются две новые соли: алюминиевые гидроксокомплексы и железные гидроксокомплексы. Оба комплекса сохраняют свойства оснований, так как их растворы обладают щелочной средой.
Химические реакции между основаниями могут также приводить к образованию осадков. Например, при смешивании растворов гидроксида натрия (NaOH) и гидроксида стронция (Sr(OH)2) образуется осадок гидроксида стронция (Sr(OH)2) в виде белого порошка.
NaOH + Sr(OH)2 → Sr(OH)2 + Na+
Аналогичные реакции возможны и с другими основаниями, их результатом может быть образование различных осадков.
Таким образом, химические реакции между основаниями могут быть разнообразными и приводить к образованию новых соединений или нейтрализации их свойственной реактивности.
Специфические характеристики оснований

Одной из основных характеристик оснований является их способность образовывать гидроксидионы OH-. Гидроксидионы являются основанием самого широкого класса, известного как щелочи. Они образуются из оснований водородом и гидроксид-ионом, и их наличие в растворе делает раствор щелочью.
Основания также обладают свойством нейтрализовать кислоты. Это происходит в результате реакции между кислотой и основанием, при которой образуется соль и вода. Реакция нейтрализации оснований с кислотами является экзотермической и сопровождается выделением тепла.
Способность оснований реагировать с другими основаниями также является специфической характеристикой. В этом случае, как и при нейтрализации с кислотами, образуются соли и вода. Примером такой реакции может быть взаимодействие гидроксида натрия (NaOH) с гидроксидом калия (KOH), в результате которого образуется соль NaK и вода.
В таблице ниже приведены примеры специфических характеристик оснований:
| Основание | Специфические характеристики |
|---|---|
| Гидроксид натрия (NaOH) | Образует щелочь, способен нейтрализовать кислоты, реагирует с другими основаниями |
| Гидроксид калия (KOH) | Образует щелочь, способен нейтрализовать кислоты, реагирует с другими основаниями |
| Гидроксид аммония (NH4OH) | Образует щелочь, способен нейтрализовать кислоты, реагирует с другими основаниями |
Обладая этими специфическими характеристиками, основания играют важную роль в химических реакциях и имеют широкое применение в различных отраслях науки и техники.
Важность правильного сочетания оснований

Основания могут реагировать между собой, образуя продукты, которые могут быть полезными или вредными. Например, если сочетание оснований приведет к образованию безопасного продукта, это может быть использовано в различных сферах, таких как медицина или производство. С другой стороны, неправильное сочетание оснований может вызвать возникновение опасных или токсичных веществ.
Исключительно важно знать свойства каждого основания и его взаимодействие с другими основаниями, чтобы избежать возможных негативных последствий. Например, некоторые основания могут образовывать реактивные соединения, которые могут вызывать взрывы или отравления, если они попадут в неправильное сочетание.
Правильное сочетание оснований позволяет контролировать процессы в химических реакциях и обращаться с ними в безопасной и эффективной манере. Кроме того, правильное сочетание оснований может повысить эффективность химической реакции и улучшить качество полученных продуктов.
Чтобы добиться правильного сочетания оснований, необходимо учитывать их свойства, реакционные способности и степень их взаимодействия. Это требует комплексного подхода и глубоких знаний в области химии.
Горение оснований и его последствия

Горение оснований происходит при их контакте с кислородом или другим окислителем. Особенно легко горят металлические основания, такие как натрий, калий, литий и другие алкалиметаллы. При горении оснований происходит окисление металла, в результате чего образуется оксид металла и выделяется энергия в виде тепла и света.
Горение оснований может иметь серьезные последствия. Во-первых, при горении выделяется большое количество тепла, что может привести к пожарам и поражению людей. Во-вторых, образующиеся при горении оксиды могут быть ядовитыми или коррозионно-активными веществами, что может вызывать травмы и повреждения окружающей среды.
Одним из примеров горения оснований является горение металлического натрия. При контакте натрия с кислородом воздуха происходит интенсивное горение, сопровождающееся светом и выделением тепла. В результате образуется основа оксида натрия – щелочь и выделяется энергия. Этот процесс часто используется в пиротехнике для создания ярких огней и фейерверков.
Основания в биологических системах

Некоторые основания в биологических системах используются для обмена ионами и электролитом. Например, ионы гидроксида (ОН-) играют важную роль в процессе гомеостаза в организме. Они участвуют в обмене кальция, натрия, калия и многих других ионов, помогая поддерживать их концентрацию на оптимальном уровне.
Основания также присутствуют в биологических макромолекулах, таких как белки. Некоторые аминокислоты, которые являются основаниями, играют важную роль в структуре и функции белков. Они могут образовывать водородные связи с другими аминокислотами и молекулами, что помогает определять трехмерную структуру и свойства белка.
Кроме того, основания играют важную роль в биохимических реакциях организма. Они могут быть использованы в качестве катализаторов для многих реакций, включая гликолиз, цикл Кребса и дыхательную цепь. Они также могут служить важными компонентами ферментов, участвующих в синтезе и разрушении молекул в организме.
В целом, основания являются важными компонентами биологических систем и играют ключевую роль в многих процессах организма. Они помогают поддерживать жизненно важные функции организма, регулировать биохимические реакции и обеспечивать стабильное состояние внутренней среды.
Формирование оснований при взаимодействии с кислотами

Как правило, основания взаимодействуют с кислотами, обладающими H+ ионами. В ходе этой реакции ион H+ кислоты присоединяется к свободному электронному парам на атоме основания, образуя новую химическую связь. В результате этого процесса, образуются соль и вода.
Например, рассмотрим реакцию взаимодействия гидроксида натрия (NaOH) с кислотой соляной (HCl). В ходе этой реакции ион гидроксида (OH-) нейтрализует ион водорода (H+) кислоты, образуя соль хлорида натрия (NaCl) и воду (H2O).
NaOH + HCl → NaCl + H2O
Таким образом, взаимодействие оснований с кислотами приводит к образованию солей и воды, являющихся основными продуктами реакции.
Примеры реакций оснований
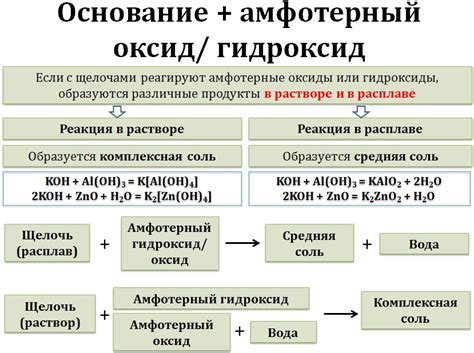
Основания могут проявлять реакцию при взаимодействии с другими основаниями. Ниже приведены некоторые примеры таких реакций:
- Реакция между гидроксидом натрия (NaOH) и гидроксидом калия (KOH). При взаимодействии этих оснований образуется раствор, состоящий из гидроксидов обоих металлов (NaOH и KOH).
- Реакция между гидроксидом кальция (Ca(OH)2) и гидроксидом алюминия (Al(OH)3). В результате этой реакции образуется осадок алюминат кальция (Ca(AlO2)2), который выпадает из раствора.
- Реакция между гидроксидом магния (Mg(OH)2) и гидроксидом цинка (Zn(OH)2). При взаимодействии этих оснований образуется осадок гидроксида магния (Mg(OH)2), который выпадает из раствора.
Это лишь некоторые примеры реакций оснований. Существуют и другие основания, которые могут реагировать между собой и образовывать различные продукты реакции. Знание этих реакций имеет большое значение при изучении химии и применении оснований в различных отраслях науки и промышленности.
Значение реакций оснований для промышленности и науки

Реакции оснований имеют огромное значение для промышленности и науки. Они играют ключевую роль во многих процессах, включая производство химических веществ, катализаторов, лекарственных препаратов и многих других продуктов.
В промышленности реакции оснований широко применяются для получения различных продуктов на основе химических соединений. Например, гидроксид натрия используется для производства стекла, мыла, бумаги, моющих средств и других продуктов. Основания также активно используются в производстве минеральных удобрений, металлов, в процессе очистки воды и сточных вод.
Реакции оснований имеют важное значение и в научных исследованиях. Они являются основой для изучения различных химических процессов и реакций, а также помогают получить новые соединения и материалы с уникальными свойствами. Например, в органической химии реакция нуклеофильной замены, основанная на реакции основания с электрофильным соединением, широко используется для синтеза сложных органических соединений.
Реакции оснований также играют значимую роль в биохимии и медицине. Они помогают изучать и понимать реакции, происходящие в организме, и на их основе разрабатываются новые лекарственные препараты. Например, некоторые лекарства, такие как противоаллергические и антигистаминные препараты, основаны на реакциях оснований с определенными соединениями в организме для блокировки определенных биологических процессов.
Таким образом, реакции оснований имеют огромное значение для промышленности и науки. Они способствуют развитию различных отраслей, помогают создавать новые продукты и материалы, а также улучшают наше понимание химических и биологических процессов.