Реакция соляной кислоты с CaO (оксид кальция) является одним из фундаментальных процессов в химии. Эта реакция представляет собой пример соединения кислоты и основания, результатом которого является образование воды и соли. Однако, перед тем как погрузиться в механизм реакции, необходимо обратить внимание на условия, при которых она может протекать.
Для реакции соляной кислоты с CaO нужны определенные условия, чтобы она могла протекать эффективно. Во-первых, необходимо обеспечить присутствие достаточного количества реагентов - соляной кислоты и CaO. Концентрация соляной кислоты должна быть достаточно высокой, чтобы обеспечить активное взаимодействие между реагентами. Также, важно контролировать температуру реакции, поскольку она может влиять на скорость и полноту протекания процесса.
Механизм реакции соляной кислоты с CaO основан на присутствии двух основных шагов: протонировании и гидратации. В первом шаге, соляная кислота отдает протон, образуя ион хлорида и образовавшуюся после отрыва протона соль кислоты. Во втором шаге, образовавшаяся соль растворяется в воде, а ион кальция из CaO присоединяется к воде, образуя гидроксид кальция. Таким образом, реакция соляной кислоты с CaO может быть представлена следующей химической реакцией: HCl + CaO = CaCl2 + H2O.
Соляная кислота: состав и свойства
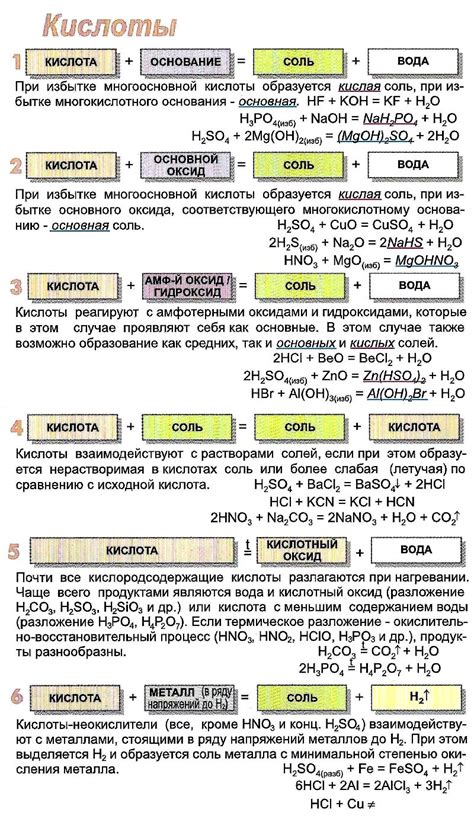
Состав соляной кислоты важен для понимания ее свойств и реакций. Молекула HCl состоит из одного атома водорода (Н) и одного атома хлора (Cl), связанных одинарной полярной ковалентной связью. Полярность этой связи делает соляную кислоту очень реакционной и способствует ее активности в различных химических процессах.
Соляная кислота обладает рядом выдающихся свойств. Во-первых, она является сильным окислителем, то есть способна окислять другие вещества. Во-вторых, она обладает кислотными свойствами и легко диссоциирует в водном растворе, образуя ион хлорида (Cl-) и протон (H+). Благодаря этому, соляная кислота обладает высокой степенью ионизации и может существовать в виде кислотного раствора с различной концентрацией.
Соляная кислота является сильным коррозионным агентом и может реагировать с различными материалами, включая металлы, оксиды, основания и некоторые органические соединения. Она широко используется в лабораториях и промышленности для различных целей, таких как обработка металлов, производство солей и использование в химическом анализе.
Важно помнить, что соляная кислота – это опасное вещество, требующее осторожного обращения и соблюдения мер безопасности при использовании.
CaO: структура и свойства

Структура кальция оксида – ионная. В кристаллической решетке CaO катионы кальция Ca2+ занимают центральные позиции, а анионы оксида O2- окружают их. Каждый катион связан с шестью анионами оксидом.
Кальций оксид обладает высокой температурой плавления (около 2570 °C) и низкой теплопроводностью. Он является твердым веществом, белого цвета.
Одно из основных свойств CaO – его щелочность. Когда кальций оксид контактирует с водой, происходит химическая реакция, при которой образуется щелочный гидроксид Ca(OH)2. Также, CaO обладает высокой растворимостью в кислотах, при растворении которых образуются соли кислот с кальцием.
Кальций оксид широко используется в различных отраслях промышленности. Он используется для производства цемента, стекла, электроники и других продуктов. Кроме того, CaO применяется в сельском хозяйстве в качестве удобрения.
Механизм реакции соляной кислоты с CaO
- Вначале происходит диссоциация соляной кислоты на ионы водорода (H+) и хлорида (Cl-).
- Далее ионы водорода реагируют с ионами оксида кальция (CaO), образуя молекулы воды (H2O) и ионы кальция (Ca2+). Эта реакция является экзотермической.
- В этой реакции ионы кальция играют роль основания, а ионы водорода - роль кислоты. Их соединение образует соль - хлорид кальция (CaCl2).
- Образовавшаяся соль растворяется в воде, образуя ионы кальция и хлорида.
Условия проведения реакции соляной кислоты с CaO зависят от желаемой скорости реакции и концентрации реагентов. Однако, для большинства случаев могут быть использованы следующие условия:
- Температура: реакция происходит при комнатной температуре (около 25°C).
- Концентрация соляной кислоты: идеальной концентрацией соляной кислоты является 6 М.
- Количество CaO: для полного протекания реакции обычно требуется стехиометрическое количество CaO, то есть в соответствии с молярным соотношением соляной кислоты и кальция.
- Время реакции: время реакции может варьироваться в зависимости от конкретных условий и реакционных параметров.
Важно отметить, что реакция соляной кислоты с CaO является быстрой и экзотермической, поэтому необходимо проводить ее с осторожностью и соблюдением мер безопасности.
Условия проведения реакции

Реакцию между соляной кислотой и CaO можно проводить при следующих условиях:
- Температура: реакцию проводят при комнатной температуре или ниже, так как она протекает достаточно быстро.
- Концентрация: обычно для реакции используют 0,1-1 М раствор соляной кислоты.
- Масса CaO: оптимальное количество CaO для реакции зависит от его массы, концентрации раствора и желаемого количества образующейся соли.
- Реакционная посуда: для реакции можно использовать прозрачную стеклянную посуду или пластиковый контейнер.
- Способ смешивания: реакцию можно проводить путем аккуратного добавления соляной кислоты к порошку CaO с помощью пипетки или шприца.
Важно помнить, что при проведении реакции соляной кислоты с CaO необходимо соблюдать меры безопасности, так как реакция сопровождается выделением газа и тепла. Рекомендуется проводить реакцию в хорошо проветриваемом помещении и носить защитные очки и резиновые перчатки.
Применение реакции соляной кислоты с CaO

Реакция соляной кислоты с CaO, также известная как реакция нейтрализации, имеет широкое применение в промышленности и лабораторных условиях. Сейчас мы рассмотрим некоторые из основных областей применения этой реакции.
Производство кальцинированной соды
Реакция соляной кислоты с CaO является одним из этапов производства кальцинированной соды (Caustic Soda), также известной как гидроксид натрия. Во время этой реакции соляная кислота реагирует с CaO, образуя газообразный оксид углерода и гидроксид кальция, который затем используется для производства гидроксида натрия.
Очистка и умягчение воды
Реакция соляной кислоты с CaO может использоваться для очистки и умягчения воды. При добавлении соляной кислоты к CaO происходит нейтрализация кальция и магния, которые являются основными причинами жесткости воды. Результатом этой реакции является образование сульфата кальция и хлорида магния, которые не образуют накипи, в отличие от карбонатов.
Производство пищевых добавок
Реакция соляной кислоты с CaO может использоваться для производства пищевых добавок, таких как кальцийцитрат и кальцияглюконат. Во время этой реакции CaO нейтрализует соляную кислоту, образуя соль кальция и воду. Полученные продукты могут использоваться в качестве источника кальция для пищевых продуктов и добавок.
Подготовка сульфата кальция
Реакция соляной кислоты с CaO может быть использована для подготовки сульфата кальция, который используется в строительной и сельскохозяйственной промышленности. В результате этой реакции CaO нейтрализует соляную кислоту, образуя сульфат кальция и воду. Сульфат кальция широко используется как добавка в цемент и удобрения, а также в процессе обеззараживания и очистки воды.
Таким образом, реакция соляной кислоты с CaO имеет много применений в различных отраслях промышленности и лабораторных условиях. Эта реакция является незаменимым инструментом в производстве различных веществ и материалов.