Масса газа - это величина, которая определяет количество вещества в газообразном состоянии.
Она является одной из важных характеристик газа и необходима для решения многих физических и химических задач.
Если вам известны объем газа и количество вещества, вы можете легко вычислить его массу.
Объем газа определяет пространство, занимаемое газом.
Он может быть выражен в литрах, кубических метрах или других единицах измерения.
Объем газа может быть измерен с использованием различных приборов, таких как мерные цилиндры или градуированные колбы.
Количество вещества - это количество молекул, атомов или ионов, содержащихся в газе.
Оно измеряется в молях и определяет количество частиц, участвующих в химической реакции или физическом процессе.
Количество вещества можно вычислить, зная молярную массу вещества и массу газа.
Общая информация о массе газа
Масса газа зависит от его количества и молярной массы. Количество вещества измеряется в молях и определяется числом молекул, атомов или ионов газа. Молярная масса выражается в г/моль и представляет собой массу одного моля газа.
Для расчета массы газа, необходимо знать его количество вещества (в молях) и молярную массу. Известное количество вещества и объем газа тоже могут понадобиться для определения массы при известной плотности газа.
Важно помнить, что масса газа может изменяться в зависимости от условий, таких как давление и температура. При изменении этих параметров, масса газа может меняться, но количество вещества остается постоянным.
Что такое масса газа?
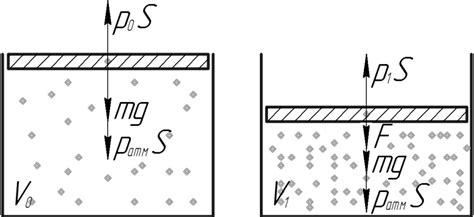
Масса газа напрямую связана с его объемом и количеством вещества по формуле: m = M * n, где m – масса газа, M – молярная масса вещества, n – количество вещества в молях.
Для определения массы газа необходимо знать его объем, выраженный в единицах объема (м3, литр), а также количество вещества, также измеряемое в молях. Обычно эти параметры известны или могут быть определены экспериментально.
Знание массы газа позволяет проводить расчеты, связанные с его использованием, например, при проведении химических реакций, в газовой аналитике, в промышленности и других областях. Также масса газа влияет на его физические и химические свойства, такие как плотность, давление, теплопроводность и др.
Для удобства работы с массой газа ее обычно измеряют в одной из основных систем единиц – СИ или СГС, однако в различных областях науки и промышленности могут использоваться другие системы единиц.
Изучение массы газа и его взаимосвязи с другими параметрами позволяет более глубоко понять свойства и поведение газового вещества, что является основой для решения различных практических задач.
Формула для вычисления массы газа
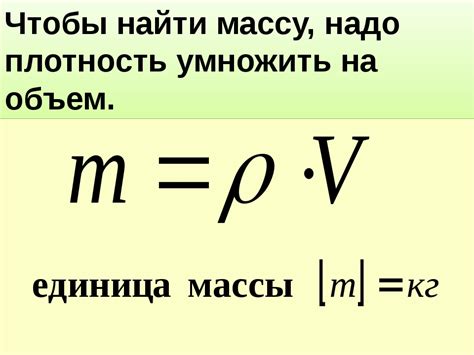
Для решения задачи по нахождению массы газа при известном объеме и количестве вещества, можно использовать формулу:
масса (m) = количество вещества (n) * молярная масса (M)
где:
- масса (m) - искомая величина, определяющая массу газа;
- количество вещества (n) - известное значение, которое указывает на количество молей газа;
- молярная масса (M) - физическая константа, значение которой зависит от химического свойства газа.
Количество вещества измеряется в молях (mol), масса - в граммах (g), молярная масса - в г/моль. Для решения задачи необходимо установить значения всех известных величин и выполнять вычисления с использованием указанной формулы.
Например, для нахождения массы газа при известном объеме и количестве вещества:
- Определите значение количества вещества (n) по имеющимся данным.
- Уточните молярную массу газа (M), обратившись к периодической таблице элементов или другому источнику.
- Подставьте значения количества вещества и молярной массы в формулу.
- Выполните вычисления и получите искомую массу газа.
Знание формулы для вычисления массы газа является важным для проведения различных физических и химических расчетов, а также для понимания основных законов и принципов, связанных с газовой фазой веществ.
Как найти массу газа

Для нахождения массы газа при известном объеме и количестве вещества необходимо использовать формулу массы газа:
- Определите известные значения: объем газа (V) в литрах и количество вещества (n) в молях.
- Используйте универсальный газовый закон (идеальный газовый закон) для нахождения молярной массы газа (M).
- Следующая формула позволяет вычислить массу газа (m), исходя из известных значений объема (V) и количества вещества (n):
m = M * n
Где:
- m - масса газа в граммах;
- M - молярная масса газа в г/моль;
- n - количество вещества в молях.
Универсальный газовый закон может быть записан в виде:
PV = nRT
Где:
- P - давление газа;
- V - объем газа;
- n - количество вещества газа;
- R - универсальная газовая постоянная;
- T - температура газа в Кельвинах.
Исходя из универсального газового закона, молярная масса газа (M) может быть найдена по формуле:
M = (molar mass of gas) = (mRT) / PV
Где:
- m - масса газа в граммах;
- P - давление газа;
- V - объем газа;
- R - универсальная газовая постоянная (0.0821 л·атм / (моль·К) или 8.314 Дж / (моль·К));
- T - температура газа в Кельвинах (для использования в силах и кельвинах).
Зная молярную массу газа и количество вещества, можно легко вычислить массу газа.
Известный объем и количество вещества
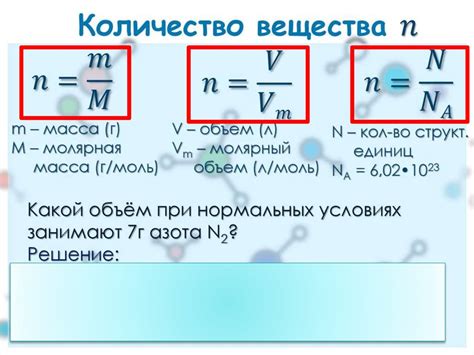
Если вам известны объем и количество вещества газа, то вы можете легко найти его массу. Для этого вам понадобятся значения объема и количества вещества, а также молярная масса газа.
Шаги для нахождения массы газа:
- Запишите известные значения объема и количества вещества.
- Найдите молярную массу газа, которую можно найти в таблице химических элементов или по формуле вещества.
- Используя формулу масса = количество вещества × молярная масса, вычислите массу газа.
Приведем пример нахождения массы газа при известном объеме и количестве вещества. Предположим, у нас есть 2 моля газа азота (N2) и его объем составляет 10 л. Молярная масса N2 равна 28 г/моль.
| Величина | Значение |
|---|---|
| Объем газа (V) | 10 л |
| Количество вещества (n) | 2 моль |
| Молярная масса (M) | 28 г/моль |
| Масса газа (m) | 56 г |
Таким образом, масса газа азота составляет 56 г при объеме 10 л и количестве вещества 2 моль.
Константы и уравнение состояния

Для выполнения расчетов по определению массы газа при известном объеме и количестве вещества необходимо учитывать ряд физических констант и использовать уравнение состояния.
Важными физическими константами, связанными с газами, являются:
- Константа Авогадро (NA), равная приближенно 6.022 × 10^23 моль^-1. Она обозначает число атомов или молекул в одном моле вещества.
- Универсальная газовая постоянная (R), имеющая значение около 8.314 Дж/(моль·К). Константа R связана с энергией и температурой газовой системы, и используется в уравнении состояния для расчетов.
Уравнение состояния объединяет различные факторы, влияющие на газовую систему, и позволяет связать массу газа (m), его объем (V), количество вещества (n) и температуру (T). В общем виде уравнение состояния можно записать следующим образом:
PV = nRT
где:
- P - давление газа в паскалях (Па)
- V - объем газа в кубических метрах (м³)
- n - количество вещества газа в молях (моль)
- R - универсальная газовая постоянная
- T - температура газа в кельвинах (К)
С помощью этого уравнения можно определить массу газа путем перестановки переменных и решения уравнения относительно m:
m = (n · molar mass) / (Molar volume)
где:
- m - масса газа в килограммах (кг)
- molar mass - молярная масса газа в килограммах на моль (кг/моль)
- Molar volume - молярный объем газа в кубических метрах на моль (м³/моль)
Используя данные константы и уравнение состояния, можно эффективно находить массу газа при известном объеме и количестве вещества, что имеет важное значение в различных областях науки и техники.
Примеры вычисления массы газа

Вот несколько примеров, как вычислить массу газа, зная его объем и количество вещества:
- Пример 1:
- Пример 2:
- Пример 3:
Пусть у нас есть газ с известным объемом 2 литра и количеством вещества 0,5 моль. Чтобы найти массу газа, нужно использовать формулу масса = объем * молярная масса. Пусть молярная масса газа равна 32 г/моль. Подставляем значения в формулу: масса = 2 л * 0,5 моль * 32 г/моль = 32 г.
Пусть у нас есть газ с объемом 4,5 литра и массой 64 г. Чтобы найти количество вещества газа, нужно использовать формулу количество вещества = масса / молярная масса. Пусть молярная масса газа равна 16 г/моль. Подставляем значения в формулу: количество вещества = 64 г / 16 г/моль = 4 моль.
Пусть у нас есть газ с известной массой 96 г и количеством вещества 6 моль. Чтобы найти объем газа, нужно использовать формулу объем = количество вещества * (константа Авогадро / 1000). Константа Авогадро равна приблизительно 6,022 * 10^23 молекул/моль. Подставляем значения в формулу: объем = 6 моль * (6,022 * 10^23 молекул/моль / 1000) = 36,132 * 10^23 литра.
Таким образом, вы можете использовать эти примеры для вычисления массы газа при известном объеме и количестве вещества. Разберитесь со значениями в вашей задаче и примените соответствующую формулу.