Законы идеального газа – одно из фундаментальных понятий физики, которые позволяют описывать поведение газового состояния на основе нескольких простых уравнений. Однако, существует некоторая особенность, которую нужно учесть при рассмотрении насыщенных паров.
Насыщенная пар – это газовое состояние, при котором фазовое равновесие достигнуто между жидкостью и ее паром при определенной температуре. В таком состоянии концентрация молекул пара достигает максимума, и дальнейшее изменение условий приводит к конденсации или испарению.
При анализе поведения насыщенных паров возникает вопрос: подчиняются ли они законам идеального газа? Ответ на этот вопрос неоднозначен и зависит от уровня детализации рассматриваемой модели. В общих чертах, изотермическое и изобарное поведение насыщенных паров можно описать с учетом законов идеального газа.
Однако, для более точного описания свойств насыщенных паров необходимо учитывать такие факторы, как взаимодействие между молекулами, изменение объема при конденсации или испарении и изменение тепловой емкости. Эти факторы могут привести к отклонениям от идеального газового закона и требуют более сложных моделей для их описания.
Исследование насыщенных пар

Однако, когда газ находится в насыщенном состоянии, его поведение становится сложнее и отличается от модели идеального газа. Насыщенные пары образуются при достижении равновесия между жидкостью и ее паром. В таком состоянии газовые частицы взаимодействуют друг с другом и с жидкостью, а их движение становится ограниченным.
Исследование насыщенных пар является важным аспектом физической химии и газовой динамики. Оно позволяет понять, какие изменения происходят в газовом состоянии при изменении давления и температуры.
Насыщенные пары не подчиняются строгим законам идеального газа, так как их перемещение ограничено в пространстве и взаимодействие между частицами и жидкостью влияет на их свойства. Тем не менее, для описания некоторых свойств насыщенных пар можно использовать некоторые элементы идеального газа, например, уравнение состояния или закон Гей-Люссака.
Исследование насыщенных пар позволяет понять и предсказать поведение газовых смесей, а также оптимальные условия для технических процессов, связанных с газами. Знание свойств и поведения насыщенных пар является основой для разработки различных технологических решений в области энергетики, химии и других отраслей промышленности.
Определение насыщенных пар
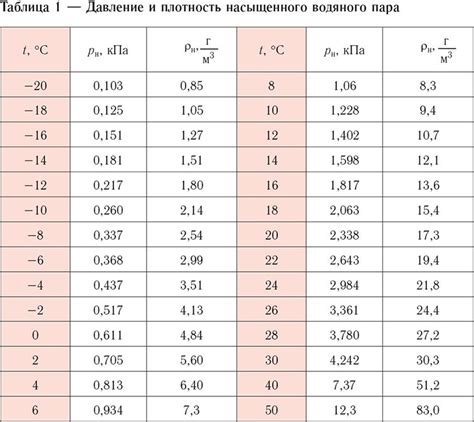
Равновесие насыщенных пар определяется давлением насыщенных паров. При повышении температуры давление насыщенных паров также возрастает. Этот параметр является характеристикой данного вещества и может быть использован для определения его физических свойств.
Законы идеального газа можно применять для насыщенных паров, так как они представляют собой гомогенную систему, в которой молекулы взаимодействуют только со стенками сосуда. Однако следует отметить, что при высоких давлениях или низких температурах аппроксимация идеального газа может быть неточной, и молекулярные взаимодействия начинают играть важную роль.
Нарушение законов идеального газа

- Высокие давления и низкие температуры: При очень высоких давлениях и низких температурах насыщенные пары могут образовывать сверхидеальное состояние. В таких условиях газы могут сильно отклоняться от идеального поведения, и их свойства могут существенно изменяться. Возникают эффекты, связанные с молекулярным взаимодействием и конденсацией.
- Критические и сверхкритические состояния: При приближении к критическим точкам или нахождении в сверхкритической области, насыщенные пары сильно отклоняются от идеального поведения. К сверхкритическим состояниям относится, например, состояние воды выше ее критической температуры и критического давления. В таких условиях происходит существенная деформация молекулярной структуры и изменение характерных свойств газов.
- Присутствие неравновесных процессов: Нарушение идеальных законов газа также может происходить при наличии неравновесных процессов, таких как химические реакции, фазовые переходы и диффузия. Эти процессы могут приводить к изменению состава газовой смеси и свойств насыщенных паров.
- Ограничения газовых законов: Идеальные законы газов, такие как закон Бойля-Мариотта и закон Шарля, предполагают, что газы не обладают массой и молекулярным объемом. Однако, насыщенные пары обладают массой и занимают определенный объем, что может приводить к нарушениям идеальных законов.
При изучении насыщенных паров важно учитывать нарушения идеальных законов газа и различия в их поведении в сравнении с идеальным газом. Это позволяет более точно описывать реальные системы и предсказывать их свойства в различных условиях.
Эксперименты и результаты

Для проверки подчиняются ли насыщенные пары законам идеального газа был проведен ряд экспериментов, в которых изучалось поведение паров при различных условиях.
В первом эксперименте было исследовано изменение объема насыщенных паров при изменении давления. Была использована специальная камера, заполненная паром, в которой с помощью поршня можно было изменять давление. Было обнаружено, что при увеличении давления объем пара уменьшается, а при уменьшении давления объем пара увеличивается. Это соответствует закону Бойля-Мариотта, который гласит, что при постоянной температуре объем газа обратно пропорционален его давлению.
Во втором эксперименте было исследовано изменение температуры насыщенных паров при изменении давления. Была использована термостатическая камера, где с помощью нагревательных элементов можно было изменять температуру пара при постоянном давлении. Оказалось, что при повышении температуры пара его давление также повышается, а при понижении температуры давление пара уменьшается. Это соответствует закону Шарля, по которому газы при постоянном объеме обратно пропорциональны их температурам.
В третьем эксперименте было исследовано изменение концентрации насыщенных паров при изменении температуры. Была использована специальная камера с сенсором концентрации пара, который позволял измерять ее изменения при различных температурах. Оказалось, что с увеличением температуры концентрация пара увеличивается, а с уменьшением температуры концентрация пара уменьшается. Это соответствует закону Гей-Люссака, который утверждает, что объемные соотношения газообразных реагентов и продуктов химической реакции с учетом их состояний можно выразить с помощью целых чисел.
Факторы, влияющие на поведение насыщенных пар
Температура: Поведение насыщенной пары зависит от ее температуры. При низких температурах молекулы жидкости движутся медленнее и испарение происходит медленнее. При повышении температуры молекулы быстрее движутся, что увеличивает вероятность и скорость их испарения.
Давление: Давление окружающей среды влияет на поведение насыщенной пары. Если давление окружающей среды увеличивается, то часть пара может снова вернуться в жидкую фазу, а если давление снижается, испарение будет происходить более активно.
Вещественные свойства: Химический состав и структура вещества также оказывают влияние на поведение насыщенной пары. Например, для веществ с более слабыми межмолекулярными силами, как алканы, насыщенные пары подчиняются законам идеального газа в большей степени, чем для веществ с сильными межмолекулярными связями, например, воды.
Наличие примесей: Примеси влияют на поведение насыщенной пары. Например, наличие нерастворимых веществ может оказывать дополнительное сопротивление испарению или приводить к образованию аэрозолей.
Площадь поверхности: Площадь поверхности, с которой контактирует жидкость, также может влиять на поведение насыщенной пары. Большая поверхность облегчает испарение и усиливает паропроницаемость, в то время как меньшая поверхность может замедлить процесс испарения.
Размеры контейнера: Размеры контейнера, в котором находится насыщенная пара, также могут влиять на ее поведение. Уменьшение размера контейнера может увеличить давление пара, что может привести к увеличению скорости его испарения.
Применение насыщенных пар

На практике, насыщенные пары находят широкое применение в различных областях. Вот некоторые способы использования насыщенных пар:
| Область применения | Примеры |
|---|---|
| Энергетика | Процессы с использованием насыщенных паровых турбин в электростанциях для производства электроэнергии. |
| Промышленность | Использование насыщенных паров в паровых котлах для нагрева и производства пара в различных процессах, таких как промышленное отопление и паровые сушилки. |
| Медицина | Автоклавы, использующие насыщенные пары для стерилизации медицинского оборудования и инструментов. |
| Пищевая промышленность | Использование насыщенных паров в процессе консервирования и стерилизации пищевых продуктов. |
| Климатические системы | Использование насыщенных паров для охлаждения и кондиционирования воздуха в кондиционерах и охладителях. |
В этих и многих других областях насыщенные пары являются незаменимым инструментом для выполнения различных технологических и промышленных процессов.