Сера – это химический элемент, который известен человечеству уже на протяжении многих веков. Его особенностью является его кристаллическая структура и устойчивость к окружающей среде. В настоящее время сера широко используется в различных отраслях промышленности и в науке.
Вопрос о том, может ли сера раствориться в воде, занимает умы многих людей. Под растворением понимается процесс, в результате которого твердое вещество, такое как соль, сахар или кислота, распадается на мельчайшие частицы, которые остаются неразличимыми для глаза.
Однако в случае с серой ситуация не так однозначна. Сера, выделившись в свободное состояние, образует кристаллические структуры, которые не могут быть полностью разрушены. Эта особенность делает серу практически нерастворимой в воде. Несмотря на то, что есть некоторое количество серы, которое способно под действием воды образовывать кислоту серную, в общем случае сера остается нерастворимой в воде.
Сера в воде: возможно ли ее растворение?

Сера представляет собой частично топливообразное вещество, состоящее из молекул, соединенных между собой двумя атомами. Методы растворения серы в воде соединены с ее окислением и превращением в кислородсодержащее соединение.
Один из способов растворения серы в воде - это использование окислительных реакций. В ходе такой реакции, сера окисляется и образует сернокислый и сульфатные ионы, которые легко растворимы в воде. Однако этот процесс требует времени и энергии.
Другой способ растворения серы в воде - это использование химических реагентов, таких как хлор или гидрохлорная кислота. Эти реагенты реагируют с серой, образуя водородсульфитные и сульфитные ионы, которые также растворимы в воде.
Как правило, для растворения серы в воде требуется повышение температуры. При этом растворение серы ускоряется, поскольку повышение температуры увеличивает кинетическую энергию молекул, что способствует разрушению энергетического барьера и образованию раствора.
| Метод | Условия реакции |
|---|---|
| Окислительные реакции | Окислительные реагенты, время, энергия |
| Химические реагенты | Хлор, гидрохлорная кислота |
| Повышение температуры | Увеличение кинетической энергии молекул |
Таким образом, растворение свободной серы в воде возможно с помощью окислительных реакций, химических реагентов и повышения температуры. Эти методы позволяют превратить молекулы серы в растворимые ионы, что облегчает их перемещение в воде.
Состав и свойства серы
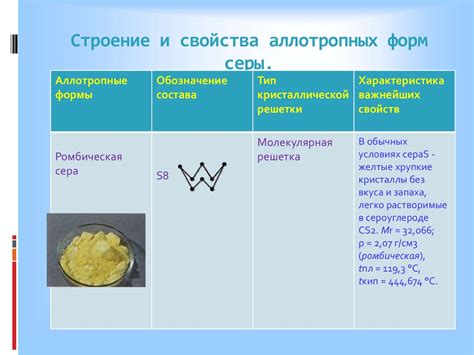
Сера является хорошим окислителем и способна вступать в реакцию с различными веществами. Она обладает и многими другими интересными свойствами:
- Высокая плотность: сера является одним из самых плотных элементов, ее плотность составляет около 2 г/см3.
- Высокая теплопроводность: у серы очень высокий коэффициент теплопроводности, что делает ее хорошим теплоносителем.
- Плохая электропроводность: сера плохо проводит электричество, поэтому является диэлектриком.
- Неполарность: сера является неполярным веществом, что влияет на ее химические свойства и растворимость.
Сера обладает также специфическим запахом, что делает ее легко узнаваемой. Она используется во многих отраслях промышленности, включая производство удобрений, пластиков, резиновых изделий и многое другое.
Физические свойства воды

1. Температура плавления и кипения: Вода плавится при 0°C и кипит при 100°C (при нормальных атмосферных условиях). Это позволяет воде существовать в трех агрегатных состояниях: твердом, жидком и газообразном.
2. Удельная теплоемкость: Вода обладает высокой удельной теплоемкостью, что означает, что она может поглощать и выпускать большое количество тепла без существенного изменения своей температуры. Это свойство позволяет воде уравновешивать климат и поддерживать более стабильную температуру в окружающей среде.
3. Плотность: Вода имеет наивысшую плотность при 4°C. При передаче тепла вода изменяет свою плотность, что влияет на циркуляцию водной массы в океанах и воздушного потока в атмосфере.
4. Поверхностное натяжение: Вода обладает высоким поверхностным натяжением, что позволяет ей образовывать капли и пленки на поверхности. Это важно для растений, насекомых и других организмов, которые используют это свойство для переживания и защиты.
5. Растворительная способность: Вода является отличным растворителем для большинства веществ, особенно для поларных соединений. Благодаря этому свойству вода способствует химическим реакциям и позволяет организмам передвигать и поглощать необходимые вещества.
Эти физические свойства делают воду уникальным и важным компонентом для жизни на Земле. Без воды жизнь, как мы ее знаем, не была бы возможной.
Взаимодействие серы и воды
Однако, при нагревании сера начинает расплавляться и реагировать с водой, образуя сероводород и серную кислоту. Реакции происходят по следующим уравнениям:
1) S(s) + H2O(l) → H2S(g) + SO2(g)
2) SO2(g) + H2O(l) → H2SO3(aq)
Образовавшийся сероводород является ядовитым газом с запахом гниющих яиц. Серная кислота, в свою очередь, является сильным окислителем и может вызывать ожоги при контакте с кожей.
Из-за слабого взаимодействия между серой и водой, образовавшийся сероводород и серная кислота обычно выделяются в виде паров или газов. Они могут присутствовать в атмосфере, вызывая неприятный запах и загрязняя окружающую среду.
Итак, сера и вода могут взаимодействовать при нагревании, образуя сероводород и серную кислоту, однако, в целом, они плохо смешиваются и образуют двухфазную систему.
- С запредельной концентрацией серы в воде она не растворяется, образуя осадок или выпадает в виде кристаллов.
- При небольшом содержании серы в воде она может растворяться и образовывать раствор, однако растворимость серы в воде невелика.
- Температура оказывает влияние на растворимость серы в воде: чем выше температура, тем лучше сера растворяется.
- Растворимость серы в воде может быть увеличена при наличии растворителей, таких как серная кислота или серный ангидрид.
- Сера может реагировать с другими веществами в воде, образуя сульфиды и другие соединения.