Оксиды – это одна из важнейших групп неорганических соединений, которые широко распространены в природе. Они играют важную роль в химических и аналитических процессах, что делает их изучение необходимым для любого учащегося 8 класса. Одним из важных аспектов в изучении оксидов является определение их вида. На первый взгляд, определение вида оксида может показаться сложным заданием, однако существуют несколько основных способов, которые позволят легко и точно определить его химический состав.
Первый способ - это определение вида оксида по его наименованию. Каждый вид оксида имеет свое уникальное название, которое позволяет сразу же определить его химическую формулу. Например, оксид калия обозначается как К2О, оксид меди - CuО, оксид железа - FeО. Знание основных оксидов и их наименований позволит быстро и точно определить вид оксида.
Третий способ - это использование свойств оксидов для их определения. Каждый вид оксида обладает своими характерными свойствами, такими как растворимость в воде, цвет, величина pH и другие. Изучение свойств оксидов позволяет точно определить их вид. Например, оксиды летучие, которые при нагревании разлагаются с образованием газа, можно определить по их запаху и поведению при нагревании. Такие свойства помогут установить вид оксида.
Оксиды: что это?

Оксиды могут быть представлены различными элементами, такими как металлы и неметаллы. Некоторые из наиболее известных оксидов включают оксид железа (Fe2O3), оксид углерода (CO2) и оксид азота (NO2).
Оксиды часто встречаются в естественном виде как руды металлов. Они могут быть получены в результате реакции металлов с кислородом или окислением неметаллов.
Одним из способов классификации оксидов является разделение их на кислые и основные оксиды. Кислые оксиды образуют кислоты при реакции с водой, а основные оксиды образуют основания.
Кроме того, оксиды могут быть использованы в различных отраслях промышленности, например, в производстве стекла, металлургии и сельском хозяйстве.
- Оксиды широко используются в производстве керамики и эмали.
- Оксиды могут использоваться в качестве катализаторов в химических реакциях.
- Некоторые оксиды, такие как оксид азота, могут быть использованы как азотные удобрения в сельском хозяйстве.
Определение вида оксида может проводиться с помощью различных химических методов, таких как растворение в воде, реакции с кислотами или основаниями, анализ физических свойств и признаков соединения.
Оксиды: классификация
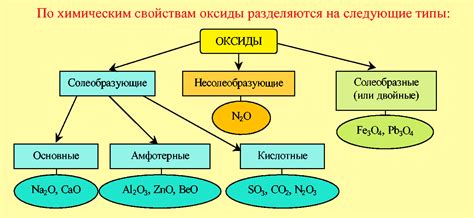
Оксиды могут быть классифицированы в зависимости от состава и свойств. Некоторые из основных классов оксидов:
| Класс оксида | Состав | Примеры |
|---|---|---|
| Металлические оксиды | Металл + кислород | оксид железа (Fe2O3), оксид меди (CuO) |
| Неметаллические оксиды | Неметалл + кислород | оксид углерода (CO2), оксид серы (SO2) |
| Многоосновные оксиды | Кислород + несколько элементов | оксид алюминия и кремния (Al2O3, SiO2) |
Классификация оксидов позволяет лучше понять их свойства и реактивность. Каждый класс оксида имеет свои особенности и применение.
Изучение оксидов и их классификации является важной частью обучения химии в 8 классе. Понимание основных классов оксидов поможет вам лучше понять химические реакции и применение оксидов в реальной жизни.
Как определить вид оксида 8 класс

Существует несколько способов определить вид оксида:
1. Анализ состава и названия
Изучите химический состав оксида и его название. Обратите внимание на присутствие металла и кислорода в соединении. Например, оксид меди (II) содержит металл медь и кислород, а оксид углерода (IV) содержит металл углерод и кислород.
2. Физические свойства
Изучите физические свойства оксида, такие как цвет, состояние (газообразный, жидкостный или твердый), плотность и температура плавления. Некоторые оксиды имеют характерные свойства, которые могут помочь в их идентификации.
3. Химические свойства
Изучите химические свойства оксида, такие как реакции с кислотами, основаниями и водой. Некоторые оксиды могут образовывать кислотные или основные растворы при реакции с водой, что может указывать на их принадлежность к определенному виду.
Важно помнить, что для точного определения вида оксида может потребоваться проведение более сложных химических анализов и использование специализированного оборудования. Если у вас возникли трудности, лучше обратиться к своему учителью или использовать специализированную литературу.
Надеемся, что эти советы помогут вам определить вид оксида и лучше разобраться в его свойствах и реакциях.
Основные способы определения оксида

Если вы хотите определить вид оксида, есть несколько основных способов:
- Использование названия химической формулы. Как правило, оксиды имеют названия, зависящие от элемента, с которым связан кислород. Например, оксид углерода - CO, оксид азота - NO.
- Изучение физических свойств оксида. Каждый оксид обладает своими уникальными физическими свойствами, такими как цвет, запах, плотность и т.д. Например, оксид железа (III) - красный порошок, оксид углерода - безцветный газ.
- Проведение химических реакций. Некоторые оксиды проявляют специфические химические свойства, которые можно использовать для их определения. Например, оксид алюминия реагирует с кислотой, образуя соль и воду.
Важно помнить, что для точного определения вида оксида необходимо проводить специальные химические исследования с использованием лабораторного оборудования. Если вы не уверены в определении, лучше проконсультироваться с опытным химиком или преподавателем.
Полезные советы для определения оксида

Определение вида оксида может показаться сложной задачей, однако с помощью некоторых полезных советов можно легко справиться с этим заданием.
1. Изучите химическую формулу оксида. Химическая формула оксида может дать вам подсказку о его составе. Например, оксид металла обычно имеет формулу MO, где M - символ металла. Оксид неметалла часто имеет формулу X2O, где X - символ неметалла.
2. Обратите внимание на название оксида. Название оксида может содержать информацию о составе и свойствах вещества. Например, оксид железа может быть назван "оксид железа(III)", что указывает на наличие трехвалентного железа.
3. Изучите свойства оксида. Свойства оксида могут помочь определить его вид. Например, оксид неметалла обычно является кислотным и реагирует с щелочью, образуя соль и воду. Оксид металла может быть щелочным и растворяется в воде, образуя гидроксид металла.
4. Проверьте окраску оксида. Некоторые оксиды имеют характерную окраску, которую можно использовать для их определения. Например, оксид железа может иметь красно-коричневую окраску, оксид меди - зеленую, оксид свинца - желтую.
Важно помнить, что определение вида оксида требует знания основных свойств веществ и закономерностей химических реакций. Регулярное изучение химии и практические опыты помогут вам успешно определить вид оксида.
Реакции оксидов

Реакции оксидов включают образование кислот или оснований, взаимодействие с водой, окисление и восстановление других соединений.
- Образование кислот: некоторые оксиды, такие как оксид серы (SO2), оксид азота (NO2) или оксид углерода (CO2), реагируют с водой и образуют кислоты, например, серную кислоту (H2SO4), азотную кислоту (HNO3)или угольную кислоту (H2CO3).
- Образование оснований: другие оксиды, такие как оксид кальция (CaO) или оксид натрия (Na2O), реагируют с водой и образуют основания, например, гидроксид кальция (Ca(OH)2)или гидроксид натрия (NaOH).
- Взаимодействие с водой: некоторые оксиды, такие как оксид меди (CuO) или оксид железа (Fe2O3), реагируют с водой и образуют гидроксиды металлов и свободный кислород.
- Окисление: некоторые оксиды, такие как оксид серы (SO2) или оксид азота (NO2), могут окислять другие соединения, например, окисление сероводорода (H2S) до серы (S) или окисление аммиака (NH3) до азота (N2).
- Восстановление: некоторые оксиды, такие как оксид железа (Fe2O3) или оксид меди (CuO), могут восстанавливать другие соединения, например, восстановление кислорода (O2) до воды (H2O) или восстановление диоксида углерода (CO2) до углерода (C).
Реакции оксидов играют важную роль в химии и находят применение во многих промышленных процессах и ежедневной жизни.
Применение оксидов

- Промышленность: множество оксидов, таких как оксиды железа, алюминия, натрия и других, используются в промышленности для производства металлов, стекла, керамики, и других материалов.
- Электроника: оксиды, такие как оксид цинка и оксид кремния, используются в производстве полупроводниковых устройств и электронных компонентов.
- Химическая промышленность: оксиды, такие как оксиды углерода, селена и серы, играют важную роль в химических реакциях и процессах.
- Медицина: некоторые оксиды, такие как оксид азота и оксид цинка, используются в медицине в качестве лекарственных препаратов и антисептиков.
- Пищевая промышленность: некоторые оксиды, такие как оксид кальция и оксид кремния, используются в производстве пищевых добавок и консервантов.
Это лишь некоторые примеры применения оксидов, их использование в различных областях достаточно широко и разнообразно. Оксиды играют важную роль в нашей повседневной жизни и являются важными компонентами многих процессов и материалов.