Медь является одним из самых распространенных химических элементов в природе. Ее активно используют в различных сферах, включая электротехнику, строительство и медицину. Но мало кто знает, что медь может реагировать с такими обычными веществами, как соляная кислота.
Соляная кислота (хлороводородная кислота) – это сильная минеральная кислота, используемая в промышленности и лабораторной практике. Ее формула HCl говорит о том, что она состоит из атома водорода и атома хлора, связанных ковалентной связью. При контакте с медью соляная кислота вызывает определенную реакцию.
Реакция меди с соляной кислотой происходит в два этапа. Сначала медь активно реагирует с хлороводородной кислотой, выделяя газовый продукт. Образуется хлорид меди(I) и водород. Второй этап реакции заключается в превращении полученного хлорида меди(I) в хлорид меди(II). Это происходит под действием кислотной среды с отрицательным окислительно-восстановительным потенциалом.
Взаимодействие меди с соляной кислотой

2HCl + Cu → CuCl2 + H2
Реакцию можно описать следующим образом:
- Соляная кислота (HCl) диссоциирует на ионы водорода (H+) и ионы хлорида (Cl-).
- Ионы меди (Cu2+) из меди (Cu) реагируют с ионами хлорида, образуя соль меди (CuCl2).
- Освобождающиеся ионы водорода соединяются в молекулы газа водорода (H2).
Реакция является экзотермической, то есть сопровождается выделением тепла. Кроме того, она происходит достаточно быстро при комнатной температуре и не требует особых условий.
Образование соли меди (CuCl2) является основным результатом реакции. Эта соль широко используется в химической промышленности и в научных исследованиях.
Химический состав реагентов
| Реагент | Химическое название | Химическая формула |
|---|---|---|
| Медь | Медь | Cu |
| Соляная кислота | Хлороводородная кислота (раствор) | HCl |
Медь представляет собой химический элемент, химическая формула которого Cu. Соляная кислота - это раствор хлороводородной кислоты (HCl). Используемые реагенты общепринято сокращать до указанных формул. Для возможности проведения эксперимента среду можно рассматривать как разбавленный раствор соляной кислоты, в котором происходит взаимодействие с медью.
Процесс реакции
Когда медь вступает в контакт с соляной кислотой, происходит переход электронов между атомами. Молекулы соляной кислоты разлагаются, атомы водорода выходят в виде газовых пузырьков. При этом, ионы меди вступают в реакцию с ионами хлора соляной кислоты, образуя хлорид меди.
Реакция меди с соляной кислотой можно представить с помощью химического уравнения:
| 2Cu | + | 4HCl | = | 2CuCl | + | H2 |
В результате реакции образуется хлорид меди (CuCl) и молекула водорода (H2). Хлорид меди может присутствовать в виде темно-зеленого кристаллического осадка или растворяться в соляной кислоте.
Реакция меди с соляной кислотой особенно интересна не только с точки зрения химических свойств, но и с практической стороны. На основе этой реакции, например, можно выполнять различные анализы или получать различные соединения для промышленности.
Образование хлорида меди

Реакция меди с соляной кислотой приводит к образованию хлорида меди, этого важного химического соединения. Эта реакция особенно интересна и полезна в химии и промышленности.
Хлорид меди является белым кристаллическим веществом, обладающим высокой термической и химической стабильностью. Он обладает хорошей растворимостью в воде и других растворителях, что позволяет использовать его в различных промышленных процессах.
Образование хлорида меди происходит в результате реакции меди с соляной кислотой (HCl). Когда медь взаимодействует с соляной кислотой, происходит образование хлоридного ионного комплекса CuCl2-. Этот комплекс ионов является основной составляющей хлорида меди.
Реакция меди с соляной кислотой происходит по следующему уравнению:
- 2HCl + Cu → CuCl2 + H2↑
В ходе реакции образуется хлорид меди и выделяется водород. Образовавшийся хлорид меди может быть использован в различных химических процессах, включая синтез органических соединений и производство других соединений меди, таких как сульфат меди или нитрат меди.
Таким образом, образование хлорида меди в результате реакции меди с соляной кислотой имеет большое значение в химии и промышленности.
Выделение газа хлора

При реакции меди с соляной кислотой образуется газ хлор. Процесс выделения газа хлора происходит следующим образом:
1. Медь взаимодействует с соляной кислотой по следующей реакции:
| Медь (Cu) | + | Соляная кислота (HCl) | → | Хлор (Cl2) | + | Медный(II) хлорид (CuCl2) |
2. Образовавшийся хлор выделяется в виде газа, который можно собрать в специальном сосуде.
3. Газ хлор имеет зеленовато-желтую окраску и характерный запах. Он очень ядовит и является сильным окислителем.
4. Выделенный газ хлор можно использовать в различных отраслях промышленности, включая производство пластиков, белил и дезинфицирующих средств.
Таким образом, реакция меди с соляной кислотой позволяет получать газ хлор, который обладает различными применениями в промышленности.
Влияние концентрации соляной кислоты

Одновременно повышение концентрации соляной кислоты может вызвать растворение меди в реакционной среде. Причина этого явления заключается в возникновении прямой гальванической реакции между медью и ионами H+, в результате которой медь окисляется и переходит в ионы Cu2+. Это может привести к уменьшению количества свободной меди в растворе и снижению скорости реакции.
Таким образом, влияние концентрации соляной кислоты на реакцию с медью может быть двояким. С одной стороны, повышение концентрации может привести к активации реакции и увеличению количества образующихся продуктов. С другой стороны, слишком высокая концентрация может вызвать растворение меди и уменьшение скорости реакции. Подбор оптимальной концентрации соляной кислоты является важным шагом при проведении эксперимента.
Образование хлористого ионного комплекса
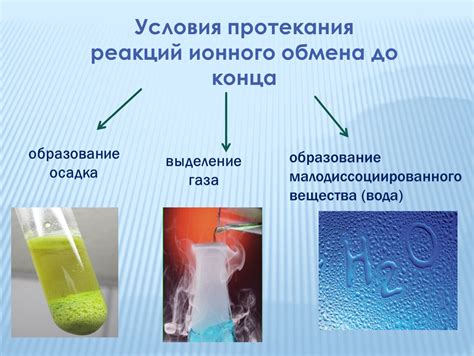
Ионы хлора, в свою очередь, образуют комплекс с ионами меди, образуя хлористый комплекс меди. Ионы хлора и ионы меди соединяются электростатическими силами, образуя стабильный комплекс.
Хлористый ионный комплекс меди обладает определенными свойствами и может использоваться в различных химических реакциях и процессах.
Образование хлористого ионного комплекса является одной из особенностей реакции меди с соляной кислотой и важным результатом этого процесса.
Итоги реакции меди с соляной кислотой

Медь может иметь разные степени окисления (Cu+ и Cu2+), поэтому в реакции меди с соляной кислотой может образовываться различное количество и типы продуктов. Обычно в реакции меди с соляной кислотой образуется хлорид меди (CuCl2), который растворяется в воде. Водород, выделяющийся при реакции, образует пузырьки исключительно легче воздуха и может быть легко собран или замечен.
Итак, результатами реакции меди с соляной кислотой являются образование хлорида меди (II) и выделение водорода:
Cu + 2HCl → CuCl2 + H2
Реакция меди с соляной кислотой является учебным примером типовой кислотной реакции, которая позволяет изучать химическую активность и свойства металлов. Благодаря этой реакции, можно получить соль меди, которая может быть использована в других химических процессах и экспериментах.
Кроме того, реакция меди с соляной кислотой может найти применение в промышленности и технологиях, например, в гальваническом покрытии медью для защиты от коррозии или в производстве электрических проводов и различных электронных устройств.
Таким образом, реакция меди с соляной кислотой имеет широкие прикладные и образовательные аспекты, и ее изучение является важным в химической науке и промышленности.