Атом, как мы знаем, является основным строительным блоком материи. Каждый атом имеет свою массу, которая определяет его свойства и характеристики. Но как найти массу отдельного атома? В этой статье мы рассмотрим формулу и приведем примеры расчета массы атома.
Масса атома измеряется в атомных единицах массы (Да), которые обозначаются символом "а. е. м.". Для расчета массы атома необходимо знать массовое число и атомное число элемента. Массовое число обозначает общее количество протонов и нейтронов в атоме, а атомное число - количество протонов.
Формула для расчета массы атома выглядит следующим образом: масса атома = (массовое число - атомное число) * 1 Да. Например, для атома кислорода с массовым числом 16 и атомным числом 8, масса атома будет равна (16 - 8) * 1 Да = 8 Да.
Масса атома: что это и почему важно знать
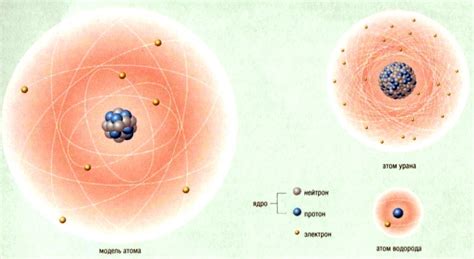
Масса атома измеряется в атомных единицах массы (а.е.м.) или в граммах. Важно отметить, что масса атома не является постоянной величиной, так как она может варьироваться для разных изотопов данного элемента. Изотопы имеют различное количество нейтронов, что приводит к изменению массы атома.
Знание массы атома позволяет проводить расчеты в химических реакциях, определять степень очистки материалов, а также изучать свойства элементов и соединений. Благодаря этому понятию мы можем точно определить количество вещества, которое требуется в реакции, и контролировать процессы, связанные с превращением веществ.
Например, при расчете количества вещества в реакции мы используем формулу: масса = количество атомов × масса атома. Пример такого расчета: если нам необходимо выяснить, сколько массы кислорода содержится в 10 атомах кислорода, мы умножаем количество атомов на его массу и получаем итоговую массу. Зная массу атома, мы можем легко рассчитать количество вещества в любой реакции.
Таким образом, знание массы атома является необходимым для проведения численных расчетов в химических и физических процессах. Оно позволяет нам понять, какие количества вещества участвуют в реакциях и как они взаимодействуют друг с другом. Поэтому изучение массы атома является основой для понимания микромира и его строения.
Формула расчета массы атома

Масса атома выражается в атомных единицах массы (а.е.м.) или делянке этих единиц (микроа.е.м.). Для расчета массы атома можно использовать следующую формулу:
Масса атома = Масса протона + Масса нейтрона
Масса протона составляет около 1,0073 а.е.м., а масса нейтрона примерно равна 1,0087 а.е.м. Следовательно, масса атома водорода (состоящего из одного протона) будет равна 1,0073 а.е.м., а масса атома гелия (содержащего двух протонов и двух нейтронов) составит 4,0026 а.е.м.
Таким образом, формула расчета массы атома позволяет определить величину, характеризующую атомный состав вещества и его химические свойства.
Примеры расчета массы атома для разных элементов

Масса атома = количество протонов + количество нейтронов
Давайте рассмотрим несколько примеров расчета массы атома для разных элементов:
Пример 1: Кислород (O)
Кислород имеет атомный номер 8, что означает, что у него 8 протонов в ядре. Массовое число кислорода равно около 16, так как у него есть 8 нейтронов. Следовательно, масса атома кислорода составляет 8 + 8 = 16.
Пример 2: Углерод (C)
Углерод имеет атомный номер 6, поэтому у него 6 протонов. Масса углерода может быть различной, так как у него есть разные изотопы с разным количеством нейтронов. Самый распространенный изотоп углерода имеет массовое число 12, что означает, что у него есть 6 нейтронов. Таким образом, масса атома углерода составляет 6 + 6 = 12.
Пример 3: Золото (Au)
Золото имеет атомный номер 79, поэтому у него 79 протонов. Самый стабильный изотоп золота имеет массовое число 197, что означает, что у него 118 нейтронов. Следовательно, масса атома золота составляет 79 + 118 = 197.
Это лишь несколько примеров расчета массы атома для различных элементов. Важно помнить, что у некоторых элементов может быть несколько изотопов с разными массами, поэтому масса атома может варьироваться.