Гибридизация - это понятие, которое используется в химии для описания орбиталей, в которых находятся электроны в молекуле. Гибридизация орбиталей влияет на геометрию молекулы и определяет ее свойства.
Давайте рассмотрим молекулу CaCl2, состоящую из атома кальция (Ca) и двух атомов хлора (Cl).
Шаг 1: Определение общего количества электронов в молекуле
Первым шагом определим общее количество электронов в молекуле CaCl2. Атом кальция имеет 20 электронов, а атомы хлора - по 18 электронов каждый. Общее количество электронов в молекуле будет равно:
20 электронов (Ca) + 2 * 18 электронов (Cl) = 56 электронов
Шаг 2: Определение гибридизации центрального атома

В молекуле CaCl2 атом кальция является центральным атомом. Поскольку у атома кальция 2 электрона, необходимо рассмотреть тип его гибридизации.
Атом кальция в состоянии основного энергетического уровня имеет электронную конфигурацию [Ar]4s2. При гибридизации один из s-орбиталей и две из p-орбиталей должны взаимодействовать. В данном случае, для образования связей с двумя атомами хлора, гибридизируются s-орбиталь и одна из p-орбиталей атома кальция.
Таким образом, гибридизация атома кальция в молекуле CaCl2 - sp-гибридизация. Это означает, что сформированные гибридные орбитали имеют характеристики обоих типов орбиталей (s и p).
Шаг 3: Определение типа связей
Для определения типа связей в молекуле CaCl2 необходимо рассмотреть гибридизацию атома кальция и атомов хлора.
Гибридизированные орбитали атома кальция образуют две σ-связи с двумя атомами хлора. Таким образом, в молекуле CaCl2 присутствуют две σ-связи.
Дополнительно, электроны каждого атома хлора могут образовывать по одной π-связи с атомом кальция, используя свои p-орбитали. Таким образом, в молекуле CaCl2 присутствует две π-связи.
Таким образом, в молекуле CaCl2 атом кальция гибридизирован по типу sp. В молекуле присутствуют две σ-связи и две π-связи. Понимание гибридизации и типов связей поможет лучше понять геометрию и химические свойства молекулы.
Определение типа гибридизации
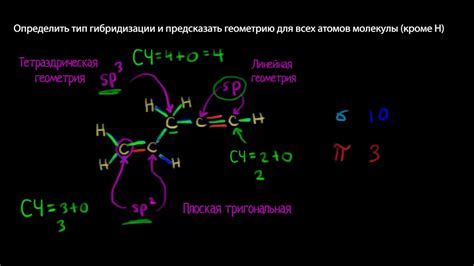
Для определения типа гибридизации в молекуле CaCl2 необходимо анализировать электронную структуру атомов кальция и хлора.
Молекула CaCl2 состоит из одного атома кальция (Ca) и двух атомов хлора (Cl). Электронная конфигурация атома кальция: 1s2 2s2 2p6 3s2 3p6 4s2. Атом хлора имеет электронную конфигурацию: 1s2 2s2 2p6 3s2 3p5.
Атом кальция отдает два электрона атомам хлора, чтобы достичь стабильности. После передачи электронов у атома кальция остаются 4 электрона на внешнем энергетическом уровне, а у атомов хлора - 8 электронов, образуя октетный внешний энергетический уровень.
Таким образом, в молекуле CaCl2 каждый атом хлора образует координационную связь с атомом кальция, а у кальция получается гибридная орбиталь SP3. Гибридизация атома кальция позволяет обеспечить оптимальное угловое расположение электронных облаков и максимальную эффективность в образовании связей с атомами хлора.