Массовая доля – это величина, выражающая отношение массы определенного вещества к общей массе раствора. Она является важным показателем в химии, так как позволяет определить концентрацию вещества в растворе. Однако, иногда может возникнуть ситуация, когда неизвестна массовая доля и требуется найти массу раствора. В таких случаях можно воспользоваться другой формулой, основанной на общем объеме раствора и плотности вещества.
Для расчета массы раствора без массовой доли необходимо знать его общий объем и плотность вещества. Важно помнить, что плотность вещества, как правило, зависит от его температуры и давления.
Для начала, следует определить плотность вещества, которое содержится в растворе. Эту информацию можно получить из справочника химических веществ или иного источника. Затем, необходимо узнать общий объем раствора, который можно измерить с помощью мерного цилиндра или другого подходящего инструмента.
Определение массы раствора без массовой доли в химии

Для определения массы раствора без массовой доли можно воспользоваться формулой:
| Обозначение | Значение |
|---|---|
| V | объем раствора (в литрах) |
| c | концентрация растворенного вещества (в моль/л) |
| M | молярная масса растворенного вещества (в г/моль) |
Массу раствора без массовой доли можно найти по формуле: масса = объем × концентрация × молярная масса.
Например, если известно, что объем раствора составляет 0,5 л, концентрация растворенного вещества равна 2 моль/л, а молярная масса растворенного вещества составляет 50 г/моль, то массу раствора можно рассчитать следующим образом: масса = 0,5 × 2 × 50 = 50 г.
Таким образом, с помощью формулы можно определить массу раствора без массовой доли в химии, исходя только из известных значений объема раствора, концентрации растворенного вещества и его молярной массы.
Измерение общей массы раствора

Для измерения общей массы раствора можно использовать аналитические весы, которые позволяют точно измерить массу как растворителя, так и растворенного вещества. Сначала необходимо взвесить пустой контейнер, а затем добавить растворитель и снова взвесить контейнер. Разница между двумя измерениями массы будет являться массой растворителя.
После этого необходимо добавить растворенное вещество и снова взвесить контейнер. Разница между двумя измерениями массы после добавления растворенного вещества будет являться массой растворенного вещества.
Однако иногда измерение общей массы раствора может быть затруднено, особенно в случаях, когда растворенное вещество имеет очень низкую концентрацию или находится в неоднородном состоянии.
В таких случаях можно использовать другие методы, например, методы оптической спектроскопии или хроматографии, для определения массы растворенного вещества. Эти методы основаны на анализе химических или физических свойств растворенного вещества и позволяют достичь более точных результатов.
Измерение общей массы раствора является важным этапом при работе с химическими растворами, поскольку позволяет определить массовые доли компонентов и провести дальнейшие расчеты и анализы.
Измерение массы растворителя
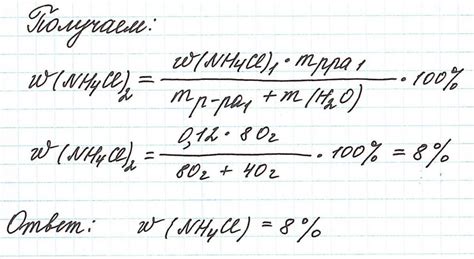
Перед началом измерений необходимо убедиться, что электронные весы находятся в исправном состоянии. Весы должны быть нулевыми, то есть показывать массу, равную нулю, когда на них не находится никакого предмета. Установите пустой сосуд на электронные весы и убедитесь, что они показывают значение 0.000 грамм.
Затем, поместите подходящую по размеру емкость на весы и нажмите кнопку "тарировать" или "нулевание". После этого на весы можно наливать растворитель.
Осторожно добавьте необходимое количество растворителя в емкость, стремясь не пересечь пределы емкости и избежать утечек. После каждого добавления растворителя подождите, пока весы перестанут менять значение и зафиксируются на одном числе.
Когда вы добавили достаточное количество растворителя, весы показывают массу, которую необходимо учесть при проведении дальнейших вычислений. Запишите эту массу и используйте ее для дальнейших расчетов, например, для определения массовой доли растворителя в химической смеси.
Важно помнить, что при измерениях массы растворителя необходимо соблюдать правила техники безопасности и использовать специальные защитные средства, такие как перчатки и очки для защиты глаз. Также следует избегать попадания растворителя на кожу и слизистые оболочки.
Вычисление массы растворенного вещества

Массовая доля растворенного вещества (массовая доля раствора) - это отношение массы растворенного вещества к массе раствора, умноженное на 100%. Формула для расчета массовой доли растворенного вещества выглядит следующим образом:
| Масса растворенного вещества | Масса раствора | Массовая доля растворенного вещества |
|---|---|---|
| m(растворенного вещества) | m(раствора) | % w/w |
Для нахождения массы растворенного вещества используем следующую формулу:
| Масса растворенного вещества | Масса раствора | Массовая доля растворенного вещества |
|---|---|---|
| m(растворенного вещества) = m(раствора) * (% w/w / 100%) | m(раствора) | % w/w |
Таким образом, чтобы рассчитать массу растворенного вещества, необходимо умножить массу раствора на массовую долю растворенного вещества, выраженную в десятичной форме.
Примечание: Важно учесть, что массовая доля растворенного вещества описывает только отношение массы растворенного вещества к общей массе раствора, а не его объему.