Молекулы - это основные строительные блоки всех веществ, которые нас окружают. Взаимодействие между молекулами играет важную роль в химии и физике, определяя свойства веществ и процессы, которые в них происходят.
Одним из интересных явлений, связанных с взаимодействием между молекулами, является усиление воздействия. Когда молекулы воздействуют на друг друга, например, при смешении двух разных веществ, возникают силы притяжения или отталкивания, которые могут усилиться или ослабиться в зависимости от различных факторов.
Усиление воздействия может проявляться на различных уровнях. На микроуровне молекулы могут взаимодействовать через слабые силы притяжения, такие как ван-дер-ваальсовы силы или водородные связи. Эти силы могут приводить к образованию агрегатов или кластеров молекул, которые имеют свойства, отличные от свойств отдельных молекул.
На макроуровне усиление воздействия может проявляться при смешении двух или более веществ. В этом случае молекулы одного вещества могут оказывать воздействие на молекулы другого вещества, вызывая изменения в их структуре или свойствах. Это может приводить к появлению новых веществ или изменению их физических и химических свойств.
Взаимодействие между молекулами и усиление воздействия имеют большое значение не только в научных исследованиях, но и в практическом применении. Понимание этих процессов позволяет создавать новые материалы, лекарственные препараты, катализаторы и многое другое. Это открывает широкие возможности для развития науки и промышленности.
Молекулы и их взаимодействие

Взаимодействие между молекулами играет ключевую роль в различных процессах, таких как химические реакции, физические изменения состояния вещества и биологические процессы. При этом взаимодействие может проявляться в разных формах, включая притяжение и отталкивание.
Притяжение между молекулами происходит благодаря различным силам, таким как ван-дер-ваальсовы силы, диполь-дипольное взаимодействие и водородные связи. Эти силы возникают из-за электрических взаимодействий между зарядами в молекулах и могут быть слабыми или сильными в зависимости от типа молекул и их структуры.
Отталкивание между молекулами может происходить из-за наличия зарядов одинакового знака или из-за столкновения молекул с высокой энергией.
Взаимодействие между молекулами может быть моделировано с использованием таблицы, где указывается тип взаимодействия и его природа. Например, в таблице можно указать, что две молекулы вступают водородные связи, которые возникают из-за разности в электроотрицательности атомов водорода и другого элемента.
| Взаимодействие | Природа |
|---|---|
| Ван-дер-ваальсовы силы | Притяжение между неполярными молекулами |
| Диполь-дипольное взаимодействие | Притяжение между полярными молекулами |
| Водородные связи | Притяжение, возникающее из-за разности в электроотрицательности |
Взаимодействие между молекулами имеет важное значение для понимания свойств и поведения вещества. Это взаимодействие может влиять на такие свойства, как теплопроводность, вязкость, плотность и температура плавления и кипения.
Исследование молекулярных взаимодействий становится все более актуальным в современной науке и технологии, так как позволяет создавать новые материалы с улучшенными свойствами и разрабатывать более эффективные процессы в различных областях, таких как фармацевтика, энергетика и материаловедение.
Механизм усиления воздействия

Взаимодействие между молекулами при усилении воздействия исследуется в контексте различных процессов, таких как химические реакции, физические взаимодействия и биологические процессы. Несмотря на разнообразие этих процессов, существует общий механизм усиления воздействия.
Один из основных механизмов усиления воздействия - это синергетическое взаимодействие между молекулами. Синергия - это явление, при котором совместное действие нескольких молекул приводит к большему эффекту, чем сумма их индивидуальных воздействий. Другими словами, взаимодействие между молекулами может привести к усилению или ускорению реакции, что может быть важным фактором в различных приложениях.
Синергетическое взаимодействие может происходить различными способами. Одним из них является физическое взаимодействие между молекулами, которое может приводить к изменению их структуры или свойств. Например, при наличии определенного количества молекул A и B, взаимодействие между ними может приводить к образованию стабильного комплекса AB, который не удалось получить при отдельном взаимодействии с молекулами A или B.
Другим примером синергетического взаимодействия является химическая реакция, в которой участвуют несколько молекул. Взаимодействие между ними может приводить к ускорению реакции или к образованию новых продуктов, которые не образуются при отдельном взаимодействии с каждой молекулой. Такие реакции могут быть важными в фармацевтической и химической промышленности, где требуется повышение эффективности процессов.
Для биологических процессов также характерно синергетическое взаимодействие. Взаимодействие между молекулами в клетках может приводить к активации определенных биологических процессов, что может быть важно для поддержания жизнедеятельности организма. Например, взаимодействие между определенными молекулами может активировать гены, регулирующие различные функции клетки.
| Примеры механизмов усиления воздействия: |
|---|
| Синергетическое взаимодействие между молекулами |
| Физическое взаимодействие, приводящее к изменению структуры или свойств молекул |
| Химические реакции с участием нескольких молекул |
| Биологические процессы, активируемые взаимодействием между молекулами |
Химические реакции между молекулами

Взаимодействие между молекулами в химических реакциях происходит с участием энергии активации, необходимой для начала реакции. Энергия активации может быть достигнута путем повышения температуры, применения катализаторов или других внешних воздействий.
В процессе химической реакции между молекулами происходят различные химические превращения, такие как образование или разрыв связей между атомами, перемещение или обмен атомов или групп атомов между молекулами и формирование новых соединений.
Реакции между молекулами могут быть эндотермическими (поглощают энергию) или экзотермическими (высвобождают энергию). В ходе реакции молекулы переходят из исходных веществ (реагентов) в конечные продукты.
Часто химические реакции между молекулами происходят в определенной последовательности, называемой механизмом реакции. Этот механизм включает промежуточные стадии, в которых образуются временные структуры, называемые промежуточными соединениями или комплексами.
Усиление воздействия на молекулы может ускорить химические реакции и повысить их эффективность. Это может быть достигнуто за счет повышения концентрации реагентов, увеличения поверхности реагирующего вещества или изменения условий окружающей среды, таких как температура и давление.
Взаимодействие между молекулами в химических реакциях обладает важными приложениями в различных областях, таких как синтез новых материалов, производство лекарств и разработка катализаторов.
В целом, химические реакции между молекулами играют ключевую роль в понимании и изучении фундаментальных принципов химии, а также имеют значительное практическое значение во многих областях человеческой деятельности.
Физическое взаимодействие между молекулами
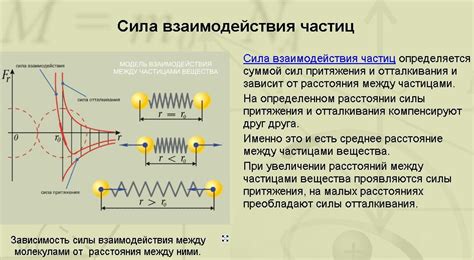
Электростатическое взаимодействие – это сила, возникающая между электрически заряженными частицами. При сближении молекул с разными зарядами происходит притяжение или отталкивание. Это взаимодействие играет важную роль в многих химических и биологических процессах.
Ван-дер-ваальсовы силы – это слабые притяжительные силы, возникающие между нейтральными молекулами, атомами или ионами. Они объясняют силу притяжения между атомами или молекулами и являются основой для понимания свойств веществ.
Диполь-дипольное взаимодействие – это взаимодействие между молекулами, у которых есть постоянный дипольный момент. Молекулы взаимодействуют через силы притяжения и отталкивания дипольных моментов. Диполь-дипольное взаимодействие играет важную роль в химических реакциях и физических свойствах многих веществ.
Влияние окружающей среды на взаимодействие молекул

Усиление воздействия между молекулами может быть сильно зависимо от окружающей среды.
При наличии растворителя, таких как вода, эти растворители могут вносить вклад в процессы взаимодействия молекул путем изменения своих свойств, таких как диэлектрическая постоянная или поляризуемость. Это приводит к усилению или ослаблению сил межмолекулярного взаимодействия.
Температура также может оказывать влияние на взаимодействие молекул. Увеличение температуры обычно приводит к увеличению энергии молекулярных движений, что может способствовать более интенсивному столкновению молекул и, следовательно, усилению взаимодействия.
Давление также может влиять на взаимодействие между молекулами. Увеличение давления может привести к сжатию молекулярного пространства, что повышает вероятность соприкосновения молекул и, таким образом, усиливает их взаимодействие.
Окружающая среда может также содержать другие вещества, которые могут реагировать с молекулами и, таким образом, влиять на их взаимодействие. Например, кислоты и основания могут изменять pH раствора, что влияет на заряд молекул и их электростатическое притяжение или отталкивание.
В общем, окружающая среда имеет большое значение для определения природы взаимодействия между молекулами и может быть использована для усиления или ослабления этих взаимодействий.
Интермолекулярные силы и их роль в процессе

Интермолекулярные силы представляют собой взаимодействия между молекулами, которые обусловлены электрическими и магнитными свойствами вещества. Эти силы играют ключевую роль в различных физических и химических процессах, определяя их скорость и эффективность.
Существует несколько видов интермолекулярных сил, включая дисперсионные, дипольные, ионно-дипольные, водородные и другие. Дисперсионные силы являются самыми слабыми из всех типов и вызваны временными изменениями электронной оболочки молекулы. Дипольные силы возникают при наличии у молекулы постоянного дипольного момента, который возникает из-за неравномерного распределения электронной плотности внутри молекулы. Ионно-дипольные силы возникают в результате взаимодействия ионов и диполей, например, в растворах солей.
Интермолекулярные силы играют важную роль во многих физических и химических процессах. Например, они определяют плотность и вязкость жидкостей, температуру их кипения и застывания, поверхностное натяжение и даже спектры поглощения и люминесценции молекул. Эти силы также проявляются в межмолекулярных взаимодействиях, в процессе образования химических связей, реакций и деструкции молекул.
Интермолекулярные силы могут быть слабыми или сильными, в зависимости от структуры и электрических свойств молекул. Например, молекулы сильно поляризованного дипольного момента могут проявлять сильные дипольные и ионно-дипольные взаимодействия. В случае водородных связей, которые являются одним из наиболее сильных типов интермолекулярных сил, молекулы должны иметь необходимые свойства, такие как наличие атома водорода, к которому могут образовываться связи с другими электроотрицательными атомами, такими как кислород или азот.
Кинетика взаимодействия молекул

Скорость взаимодействия молекул определяется множеством факторов, таких как концентрация реагентов, температура, давление и наличие катализаторов. Кинетика взаимодействия молекул позволяет прогнозировать и оптимизировать процессы, происходящие в молекулярных системах.
Одним из основных понятий в кинетике взаимодействия молекул является реакционная скорость – скорость изменения концентрации реагентов и продуктов реакции по мере прохождения времени. Реакционная скорость может быть выражена как изменение концентрации в единицу времени или как отношение изменения концентрации к изменению времени.
Для описания кинетики взаимодействия молекул часто используются математические модели, такие как уравнения реакций и уравнения скорости реакции. Модели кинетики могут учитывать как простые случаи реакций, так и сложные механизмы, включающие несколько последовательных и параллельных стадий.
Изучение кинетики взаимодействия молекул имеет важное практическое значение во многих областях науки и техники. Например, кинетика реакций используется в процессах синтеза и анализа веществ, разработке новых материалов, производстве лекарственных препаратов и оптимизации химических процессов.
Исследования кинетики взаимодействия молекул позволяют лучше понять принципы, лежащие в основе химических и физических процессов, и применять их для решения различных практических задач.
Усиление воздействия между молекулами, например, может применяться в химической синтезе для увеличения скорости реакций и повышения выхода продукта. Также это может быть полезно в катализе, где усиленное взаимодействие позволяет снизить количество используемых реакционных компонентов или повысить селективность реакции.
Взаимодействие между молекулами также может играть роль в биологических системах. Например, усиление взаимодействия может привести к силному связыванию лигандов с рецепторами, что может быть полезно в разработке лекарственных препаратов. Также это может быть важным в биомолекулярном распознавании и взаимодействии белков.
В области нанотехнологий усиление взаимодействия между молекулами может быть использовано для создания новых материалов и устройств. Например, с помощью усиленного взаимодействия можно улучшить электронные и оптические свойства материалов, что открывает новые возможности для разработки эффективных солнечных батарей, датчиков и других устройств.
Однако, несмотря на широкий потенциал и применение усиления взаимодействия между молекулами, понимание и контроль этих процессов остаются сложными задачами. Более глубокое исследование в этой области может привести к новым открытиям и развитию новых технологий.