Погружаемся в захватывающий мир холода, где взаимодействие молекул принимает особые формы. Рассмотрим явления, которые происходят с одним из самых важных веществ на Земле при температуре, которая заставляет все замирать - ноль градусов Цельсия.
Представьте себе экспериментальные условия, при которых происходит нечто уникальное. Когда температура опускается до нуля градусов, вода проходит через переломный момент, оказываясь на грани ледяной замерзшей твердости и жидкости с необычными свойствами. При этой границе силы притяжения и отталкивания молекул создают невероятные сочетания, открывая двери в изучение разных видов превращений.
На этом пути вода может метаморфироваться, меняя свою структуру и состояние с ледяного на жидкое в зависимости от многих факторов, включая давление и содержание растворенных веществ. Волшебство происходит, когда вода достигает нулевой температуры и начинает совершать свой путь к точке кипения, играя с нашими ожиданиями и тестя на прочность все наши установленные парные концепции.
Поведение воды при низкой температуре

В настоящем разделе рассматривается влияние низких температур на физические свойства воды и ее способность к изменению состояния.
При снижении температуры вода испытывает различные изменения, приводящие к изменению ее свойств, но кипение при 0 градусах Цельсия, в соответствии с общепринятым определением этого процесса, невозможно. Вместо этого, она становится менее активной и медленно переходит в более плотное состояние.
Замерзание воды в тающем состоянии, образование льда и растворение этих кристаллов при повышенной температуре являются основными механизмами, связанными с низкими температурами. Кроме того, вода обладает свойством суперохлаждения - способностью оставаться в жидком состоянии при температурах ниже точки замерзания без образования льда. Этот процесс связан с отсутствием ядер замерзания и может привести к быстрому замерзанию при воздействии стимула, например, при небольшом погружении кристалла льда или долей другой замерзнувшей воды.
Таким образом, при низких температурах вода проявляет различные свойства, отличные от обычных состояний, что обусловлено ее молекулярной структурой и взаимодействием между молекулами. Дальнейшее изучение поведения воды при низкой температуре может привести к новым открытиям и пониманию ее уникальных свойств.
Неожиданные свойства воды при нуле градусов

Погружаясь в изучение свойств воды при нуле градусов, мы обнаруживаем, что она демонстрирует необычное поведение, которое выходит за рамки нашего обыденного представления о кипении. Это явление можно описать как не всегда возможное состояние, когда вода достигает некоторых исключительных условий.
Сверхохлаждение:
Одним из интересных свойств воды при нуле градусов является явление сверхохлаждения. Вода может оставаться в жидком состоянии даже при температуре ниже точки замерзания. В таком состоянии она становится метастабильной и готова перейти в твердое состояние при малейшем возмущении.
Кристаллизация:
Когда вода сверхохлаждена и находится в метастабильном состоянии, даже небольшое воздействие может привести к мгновенной кристаллизации. Такие события могут происходить при контакте с твердыми поверхностями или при наличии замерзающего ядра, вызывающего цепную реакцию столкновений частиц, приводящих к мгновенному переходу воды в твердое состояние.
Огненная вода:
Еще одним занимательным явлением, которое можно наблюдать при нуле градусов, является возможность вспыхивания воды. При наличии определенных условий это происходит вследствие концентрации водородной сульфида или других веществ, способных испаряться и воспламеняться в контакте с кислородом из воздуха.
Огненная вода представляет собой специфическое явление, которое требует определенных условий для своего проявления и может происходить только в ограниченных областях.
Изучение свойств воды при нуле градусов открывает перед нами удивительный мир необычных физических явлений. Несмотря на то, что кипение воды при этой температуре не всегда возможно, мы можем обнаружить удивительные свойства, которые добавляют новые аспекты в понимание этого фундаментального вещества.
Реологические свойства воды при низкотемпературных условиях
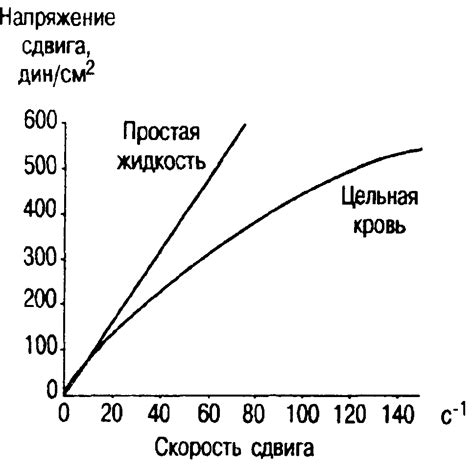
При понижении температуры вода постепенно изменяет свои физические и химические характеристики, что приводит к изменению ее потенциала. В особенности, реологические свойства воды, такие как вязкость, термоупругость и плотность, подвергаются значительному влиянию низкотемпературных условий.
- Вязкость воды при понижении температуры с увеличением плотности и уменьшением собственной движимости усиливается, препятствуя ее течению.
- Термоупругость, или способность воды к сжатию и расширению при изменении температуры, проявляется в формировании льда и обратном переходе вещества в жидкое состояние.
- Плотность воды при понижении температуры увеличивается, достигая максимума при 4 градусах Цельсия, после чего начинает уменьшаться, что является одной из причин, почему лед плавает на воде.
Соответственно, изложенные реологические свойства воды при низких температурах играют важную роль в процессах, связанных с формированием льда, образованием айсбергов и изменениями климатических условий. Кроме того, понимание этих свойств воды имеет практическое значение для таких отраслей, как гидрология, океанология и метеорология.
Своеобразные свойства воды при 0 градусов
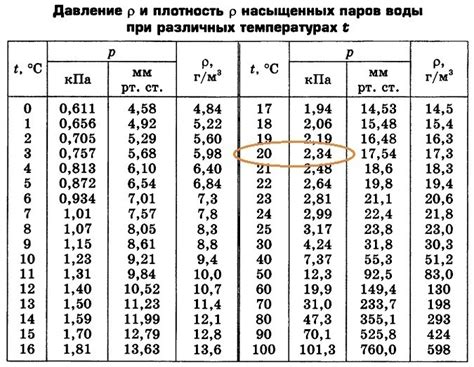
Нулевая температура, также известная как точка замерзания, обычно связывается с образованием льда. Однако, вода при 0 градусах может не только замерзать, но и кипеть, превращаясь в пар. Это специфическое свойство воды при подобных условиях вызывает удивление и требует более детального рассмотрения.
| Свойство | Синоним |
|---|---|
| Кипение | Испарение, испаряться, переход в газовую фазу |
| Нулевая температура | Точка замерзания, замерзание, лед, замораживание |
Разберемся подробнее в причинах и особенностях этого удивительного явления, чтобы лучше понять, как вода при 0 градусах может испаряться в газообразное состояние. Данная тема представляет интерес для научного исследования и имеет практическую значимость в различных областях, таких как метеорология, инженерия и физика.
Механизмы изменения агрегатного состояния воды
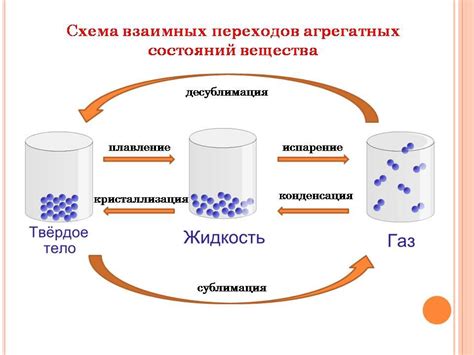
В данном разделе мы рассмотрим процессы, которые приводят к изменению агрегатного состояния воды. Мы изучим феномены, которые возникают при изменении температуры воды, и их влияние на переход воды из одного состояния в другое.
Первым механизмом, который мы рассмотрим, является плавление. Плавление - это процесс перехода воды из твердого состояния в жидкое при повышении температуры. В результате плавления молекулы воды начинают двигаться более свободно, преодолевая силы, удерживающие их в твердом состоянии. Плавление происходит при определенной температуре, которая зависит от воздействия на воду и давления.
Далее мы рассмотрим процесс испарения. Испарение - это переход воды из жидкого состояния в газообразное при повышении температуры. Под воздействием тепла молекулы воды приобретают достаточно энергии для преодоления притяжения друг к другу и переходят в состояние пара. Испарение может происходить при любой температуре, но с увеличением температуры скорость испарения увеличивается.
Еще одним механизмом, который следует рассмотреть, является конденсация. Конденсация - это процесс перехода водяного пара в газообразное состояние в жидкое при понижении температуры. При охлаждении пара его молекулы начинают сближаться и образуют капельки жидкости. Конденсация происходит при определенной температуре, которая зависит от давления и концентрации пара.
Также важным механизмом изменения агрегатного состояния является сублимация. Сублимация - это процесс, при котором вода переходит из твердого состояния в газообразное, минуя жидкое состояние. Под действием тепла молекулы льда приобретают достаточно энергии для прямого перехода в газообразное состояние без промежуточного плавления. Сублимация может происходить при низкой относительной влажности и низком давлении.
Механизм изменения состояния воды: Кипение
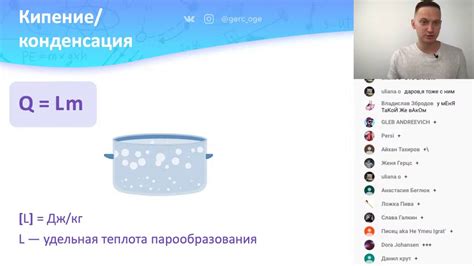
Кипение представляет собой процесс, при котором вода переходит из жидкого состояния в состояние пара. Оно происходит при достижении определенной температуры, которая может различаться в зависимости от окружающих условий и давления.
Когда вода начинает кипеть, молекулы воды приобретают достаточную энергию, чтобы преодолеть силы межмолекулярного взаимодействия и выйти из жидкого состояния. В результате образуется пар, который виден в виде пузырьков, поднимающихся к поверхности.
Температура, при которой происходит кипение, называется точкой кипения. Для воды при обычном атмосферном давлении она составляет 100 градусов Цельсия. Однако при изменении давления точка кипения может как повышаться, так и понижаться.
Кипение воды имеет большое значение для многих процессов и явлений в природе и технологии. Оно используется, например, в приготовлении пищи, производстве пара для привода турбин, а также в процессах очистки и стерилизации.
Структурные изменения при изменении температуры вещества

Когда вода подвергается нагреванию, происходит постепенное преодоление сил притяжения между молекулами. При достижении 0 градусов Цельсия, вода переходит в твердое состояние, при этом ее молекулы упорядочиваются в кристаллическую решетку. Данный процесс, называемый замерзанием, сопровождается усилением притяжения между молекулами воды.
Однако при нагревании воды свыше 0 градусов Цельсия начинается процесс кипения. В этот момент молекулы воды приобретают достаточную энергию, чтобы преодолеть силы притяжения и перейти в более подвижное состояние. Кипение сопровождается формированием пузырьков водяного пара, которые возникают в результате быстрого перехода молекул из жидкой фазы в газовую. В процессе кипения происходит нарушение упорядоченной структуры воды и ее переход в хаотическое состояние.
Интересно отметить, что при достижении точки кипения, температура воды перестает повышаться, так как в кипящей воде вся энергия, подаваемая на нагревание, расходуется на преодоление сил притяжения между молекулами, а не на повышение средней кинетической энергии. Таким образом, кипение воды при 0 градусов невозможно, так как вода находится в твердом состоянии.
Изучение структурных изменений воды при изменении температуры имеет большое значение не только для фундаментальных наук, но и для повседневной жизни. Например, знание о структуре воды при замерзании позволяет разрабатывать материалы и системы, устойчивые к образованию льда, а понимание процесса кипения помогает в различных технологических процессах, таких как приготовление пищи или производство энергии.
Вопрос-ответ

Вода при 0 градусов - возможно ли кипение?
Нет, при 0 градусов вода не кипит. Кипение воды происходит при температуре 100 градусов Цельсия, при которой жидкость превращается в пар.
Почему вода не кипит при 0 градусов?
Температура, при которой вода начинает кипеть, называется точкой кипения. Вода кипит при 100 градусах Цельсия, так как при этой температуре молекулы воды получают достаточно энергии, чтобы преодолеть силы притяжения и перейти в парообразное состояние. При 0 градусах энергии недостаточно, поэтому вода остается в жидком состоянии.
Может ли вода кипеть при 0 градусах?
Нет, при 0 градусах вода не может кипеть. Кипение – это фазовый переход жидкости в газообразное состояние при определенной температуре и давлении. При 0 градусах вода достигает своей точки замерзания и переходит в твердое состояние – лед. Для того чтобы вода начала кипеть, необходимо повысить ее температуру до 100 градусов Цельсия.
Какая температура нужна для того, чтобы вода начала кипеть?
Для того чтобы вода начала кипеть, необходимо нагреть ее до 100 градусов Цельсия. При этой температуре молекулы воды получают достаточно энергии, чтобы преодолеть силы притяжения друг к другу и перейти в парообразное состояние. Это называется точкой кипения воды.



