В мире химии не перестают удивлять нас различные соединения и вещества, обладающие уникальными свойствами и строением. Разнообразие атомов и ионов, их числа и расположение в молекуле открывают перед нами бесконечные возможности для изучения и применения в различных областях науки и промышленности.
Одним из важных параметров любого элемента является число электронов в его атоме или ионе. Число электронов, находящихся на различных энергетических уровнях, определяет его свойства и взаимодействие с другими элементами. Так, сегодня мы поговорим о числе электронов в ионе p3 и его особенностях.
Ион p3 представляет собой один из возможных заряженных состояний фосфора, химического элемента, расположенного в пятои группе периодической системы. Заряд iонов формируется за счет потери или приобретения электронов, что приводит к изменению числа электронов относительно нейтрального атома. У иона p3, таким образом, имеется достаточно высокое количество электронов, которые обладают собственными уникальными свойствами и способностями.
Определение и основные характеристики иона p3
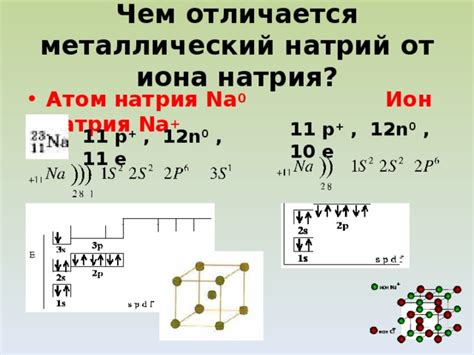
Ион p3 относится к одной из многих вариаций ионов, которые могут образоваться в химических соединениях. Этот ион является особой формой химического элемента и имеет определенное количество заряда. Именно это отрицательное заряжение делает ион p3 таким уникальным и интересным для изучения.
Одной из ключевых особенностей данного иона является его способность взаимодействовать с другими элементами и соединениями. Ион p3 способен образовывать химические связи с положительно заряженными ионами или молекулами, что позволяет ему играть важную роль в формировании различных соединений. Благодаря этому, ион p3 участвует во многих химических реакциях и процессах, влияя на их характер и результаты.
- Одним из важных свойств иона p3 является его электроотрицательность. Это свойство позволяет иону p3 притягивать к себе положительно заряженные частицы или электроны, что влияет на его способность образовывать связи с другими элементами.
- Ион p3 также обладает способностью принимать участие в реакциях окисления и восстановления. Это означает, что ион p3 может передавать электроны другим веществам, что сказывается на его влиянии на процессы окисления и восстановления.
- Еще одной характеристикой является возможность иона p3 образовывать соли. Это происходит при взаимодействии данного иона с положительно заряженными ионами или комплексами, что приводит к образованию стабильных соединений в виде солей.
- Также стоит отметить, что ион p3 обладает определенной положительной электронной плотностью. Это означает, что вокруг иона p3 сконцентрировано большое количество электронов, что влияет на его взаимодействие с окружающими частицами и соединениями.
В совокупности эти характеристики делают ион p3 важным объектом изучения в области химии и позволяют ему играть роли в различных химических процессах и реакциях.
Образование иона p3 и его особенности:
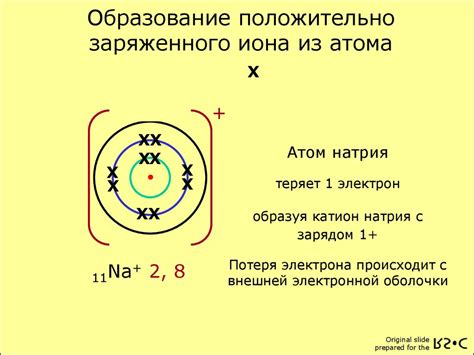
В данном разделе мы рассмотрим процесс образования иона p3, а также особенности его электронного строения.
Ион p3 образуется путем потери трех электронов атомом элемента, что приводит к изменению его заряда на +3. Такое образование иона может наблюдаться при реакциях с другими веществами или в химических соединениях.
Особенностью электронного строения иона p3 является наличие 13 электронов, распределенных по его энергетическим уровням. Такое количество электронов, как и заряд +3, делает ион p3 стабильным и способным участвовать в различных химических реакциях.
- Ион p3 обладает восемью электронами на своем внешнем энергетическом уровне, что делает его аналогом атома азота (N) в периодической системе элементов.
- Из-за наличия толстой оболочки внутренних электронов, ион p3 обладает эффективной зарядовой оградой, которая влияет на его химическую активность и реакционную способность.
- Ион p3 является трехвалентным, что означает его способность приобретать три отрицательных заряда или образовывать связи с тремя атомами других элементов.
Ион p3 играет важную роль в химии и может образовывать соединения с различными элементами, обладающие разнообразными свойствами и применениями в науке и промышленности.
Взаимодействие иона p3 с другими веществами: основные химические свойства
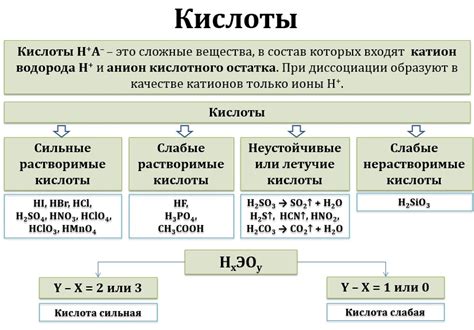
У иона p3, который представляет собой ион фосфора со степенью окисления +3, имеется ряд важных химических свойств, которые определяют его поведение при взаимодействии с другими веществами. Эти свойства могут оказывать значительное влияние на химические реакции, в которых участвует данный ион.
Одним из основных свойств иона p3 является его фосфорная натура, которая проявляется в возможности образования ионовосстановительных реакций. Ион p3 может эффективно окисляться до иона p5, образуя фосфатные соединения. Таким образом, ион p3 может служить донором электронов в реакциях окисления.
Взаимодействие иона p3 с кислородом также является важным аспектом его химических свойств. Ион p3 способен реагировать с кислородом, образуя фосфатные соединения, такие как фосфаты металлов или органические фосфорные соединения. Это обуславливает его участие в процессах фосфорного обмена в организмах живых существ и его значимую роль в биохимических процессах.
Кроме того, ион p3 способен образовывать ионные соединения с различными металлами. При этом ион p3 может выступать в роли лиганда, образуя стабильные комплексы с металлами. Такие комплексы могут обладать специфическими свойствами, которые могут применяться в различных областях химии и технологии.
В целом, химические свойства иона p3 при его взаимодействии с другими веществами представляют собой важный аспект изучения его роли и применения в различных химических процессах. Они позволяют предсказывать и объяснять поведение данного иона в различных химических системах и расширять его применение в различных областях науки и технологии.
| Примеры веществ, взаимодействующих с ионом p3 | Результат взаимодействия |
|---|---|
| Кислород | Образование фосфатных соединений |
| Металлы | Формирование ионных соединений и комплексов |
Значение иона p3 в природе и в промышленности. Практическое применение

Ион p3, известный также как трехвалентный положительный ион, играет важную роль как в природных процессах, так и в различных промышленных сферах. Будучи химическими частицами, эти ионы обладают определенными свойствами и могут быть использованы в разных практических целях.
В природе ион p3 может образовываться в результате естественных химических процессов, таких как окисление ионов металлов. Он также может быть наблюдаемым продуктом различных химических реакций в атмосфере, водах и почве. Наличие ионов p3 может значительно влиять на различные экологические процессы, такие как циклы веществ и биологическая активность организмов.
В промышленности трехвалентные положительные ионы широко используются в различных технологических процессах. Ион p3 может использоваться в качестве катализатора для ускорения различных химических реакций, таких как производство пластмасс или процессы фармацевтической промышленности. Благодаря своим свойствам, ион p3 может также быть применен в электропромышленности, например, для создания эффективных и стабильных аккумуляторов.
Практическое использование иона p3 обладает значительным потенциалом для разных отраслей. Эта химическая частица продолжает вызывать интерес у ученых и инженеров, и дальнейшие исследования могут привести к новым и инновационным приложениям. Понимание значимости и свойств иона p3 в природе и в промышленности помогает нам лучше понять и использовать его потенциал в нашей повседневной жизни.
Вопрос-ответ

Что такое ион p3 и сколько электронов в нем?
Ион p3 представляет собой ион фосфора со знаком заряда +3. В ионе p3 находится 10 электронов, так как фосфор имеет 15 электронов в нейтральном состоянии, а при наличии заряда +3 теряет 3 электрона, оставляя 10.
Как образуется ион p3?
Ион p3 образуется путем потери трех электронов фосфором. Когда фосфорная атомная оболочка переходит из нейтрального состояния в ионное состояние, три электрона покидают его оболочку, создавая положительный заряд +3.
Какая электронная конфигурация у иона p3?
Ион p3 имеет следующую электронную конфигурацию: 1s2 2s2 2p6. Это означает, что во внешней оболочке у иона p3 находятся 6 электронов.
В чем отличие электронной конфигурации иона p3 от нейтрального атома фосфора?
Нейтральный атом фосфора имеет следующую электронную конфигурацию: 1s2 2s2 2p6 3s2 3p3, что означает, что у нейтрального фосфора во внешней оболочке находятся 5 электронов. Однако, при образовании иона p3, фосфор потерял 3 электрона, что изменило его электронную конфигурацию на 1s2 2s2 2p6. Теперь во внешней оболочке иона p3 находятся 6 электронов.



