На первый взгляд, можно полагать, что молекулы, являющиеся строительными блоками веществ, должны иметь сходные размеры, так как химические реакции и взаимодействия зависят от близости молекулярных размеров. Однако, чем глубже мы исследуем данную тему, тем больше становится ясным, что в мире химии существует невероятная разнообразность молекулярных размеров.
Что влияет на размер молекул в различных веществах?

Когда мы говорим о размере молекул в различных веществах, мы не можем не учитывать то, что определенные факторы могут оказывать влияние на этот параметр. Некоторые вещества имеют молекулы с большими размерами, в то время как другие имеют молекулы меньшего размера. Однако, что же на самом деле определяет размер молекул в веществах?
Размеры молекул как ключевой параметр
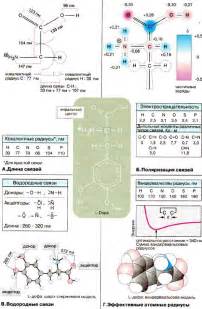
При анализе размеров молекул можно уловить сходства и различия между разными веществами. Данный параметр позволяет выделить общие особенности и закономерности, определяющие поведение веществ в различных условиях. Большой размер молекулы может указывать на сложные структуры вещества, а маленький размер может говорить о простоте его состава.
- Один из важных факторов, влияющих на размеры молекул, является количество и тип атомов в молекуле. Молекулы, состоящие из большого числа атомов, как правило, имеют больший размер, чем молекулы с меньшим числом атомов.
- Форма молекулы также оказывает влияние на ее размеры. Молекулы с круглой формой обычно более компактны и меньше по размерам, в то время как молекулы с более сложной формой могут иметь более протяженную структуру.
- Различные связи между атомами в молекуле также влияют на ее размер. Например, двойная связь между атомами может приводить к укорачиванию молекулы, в то время как наличие водородных связей может значительно увеличивать ее размеры.
- Физические условия, в которых находится вещество, также могут влиять на размеры молекул. Температура, давление и наличие растворителей могут изменять размер молекулы и ее структуру.
Таким образом, понимание размеров молекул является ключевым параметром в изучении структуры и свойств веществ. Он позволяет выявить сходства и различия между разными веществами, а также предсказать и объяснить их поведение в различных условиях.
Зависимость размеров молекул от химического состава: особенности и вариации
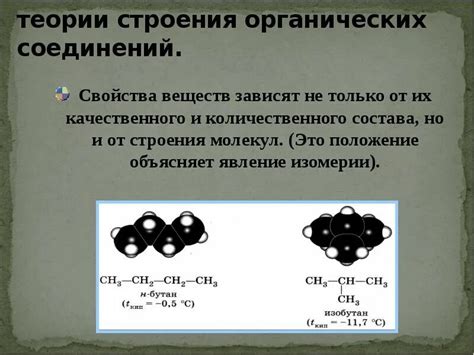
Каждое вещество, будь то жидкость, газ или твердое вещество, имеет свой уникальный химический состав, обусловленный различными атомами и связями между ними. Стремительное развитие науки позволяет нам понять, что у этих веществ также есть некая структура, именуемая молекулами.
Интересно отметить, что размеры и формы молекул могут варьироваться в зависимости от химического состава вещества. Одни молекулы могут быть крупнее и более сложными, другие - мельче и простыми. Это объясняет наличие различных свойств и характеристик у разных веществ.
- Молекулы веществ, богатых ионными связями, часто обладают большими размерами. В таких веществах, атомы соединяются друг с другом за счет электростатического притяжения зарядов и образуют крупные и сложные структуры.
- Молекулы, в которых преобладают ковалентные связи, могут представлять собой более компактные и устойчивые структуры. В таких веществах, атомы соединяются путем обмена электронами и формируют молекулы меньшего размера и более простой архитектуры.
Очевидно, что зависимость размеров молекул от химического состава вещества является непосредственной и важной. Исследования в этой области позволяют нам более глубоко понять свойства и особенности различных веществ, открывая новые перспективы для применения в науке и технологии.
Связи между атомами и распределение объемов веществ
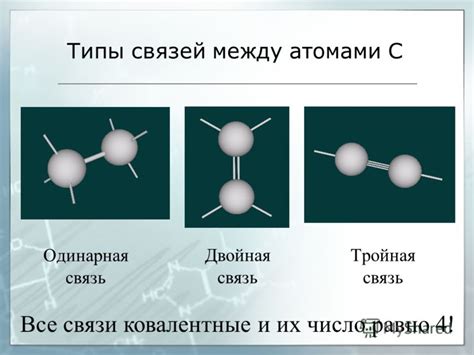
Молекулы образуются путем соединения атомов, которые взаимодействуют друг с другом с помощью электростатических сил. В результате этого взаимодействия образуются различные типы молекулярных связей, такие как ионные связи, ковалентные связи, металлические связи и др. Каждый тип связи обладает своими особенностями, которые влияют на структуру и объем вещества.
Сильные молекулярные связи, такие как ионные и ковалентные, создают компактные структуры, где атомы расположены близко друг к другу. Это приводит к сравнительно малым объемам веществ, так как межатомные расстояния оказываются небольшими. При этом, такие связи позволяют образование твердых веществ с высокой плотностью и точками плавления/кипения.
С другой стороны, слабые молекулярные связи, такие как ван-дер-ваальсовы, гидрофобные и дисперсионные связи, создают более разреженные структуры, где атомы находятся на более большом расстоянии друг от друга. Это приводит к увеличению объема вещества. Благодаря слабым связям, молекулы могут легко разделяться и перемещаться, что является причиной низких точек плавления/кипения и более высокой подвижности вещества.
Таким образом, молекулярные связи играют важную роль в определении объемов веществ. Различные типы связей создают разные структуры и интермолекулярные взаимодействия, что приводит к различиям в объемах веществ и их физических свойствах.
Влияние изменения температуры на размерности частиц в различных веществах
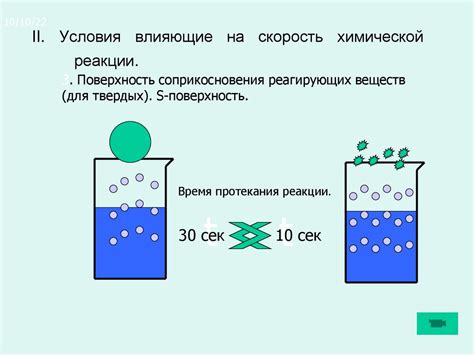
Перепады температуры оказывают значительное воздействие на величину и форму молекул в разных материалах. Повышение температуры может привести к расширению молекулярной сетки вещества, что сопровождается увеличением объема частиц. Такой процесс может быть обратимым или необратимым, в зависимости от свойств конкретного вещества.
Взаимодействие температуры и размерностей частиц наблюдается в различных материалах. Например, при повышении температуры воды, молекулы начинают двигаться более энергично, что приводит к разрыву водородных связей между ними и расширению объема. В то же время, некоторые материалы проявляют обратное поведение: с повышением температуры, молекулы сжимаются и их объем уменьшается.
Влияние температуры на размерности частиц может быть использовано для целей материаловедения и в промышленности. Изучение изменения размеров молекул при различных температурах позволяет определить точку перехода фаз, изменить свойства материалов или разработать новые материалы с заданными характеристиками.
| Вещество | Изменение объема при увеличении температуры |
|---|---|
| Вода | Увеличение объема при повышении температуры |
| Стекло | Уменьшение объема при повышении температуры |
| Металлы | Незначительное изменение объема при повышении температуры |
Научите миханизмы различия между газами и жидкостями в контексте объема и размеров их составных частиц

Глубже погрузившись в изучение свойств газов и жидкостей, мы обращаем внимание на их молекулярное устройство. Но имеют ли эти два типа вещества схожие или различные объемы молекул? В данном разделе мы разберемся, насколько похожи или отличаются между собой газы и жидкости в отношении размеров своих составных частиц.
Газы
Газы представляют собой агрегатное состояние веществ, отличающееся своей высокой подвижностью и расположением между молекулами, которые находятся на довольно больших расстояниях друг от друга. Газовые молекулы характеризуются отсутствием определенной формы и объема, они свободно перемещаются и сталкиваются друг с другом, что создает давление и объем газа. Размеры молекул газов находятся настолько небольших, что их можно сравнить с размерами атомов или ионов.
Жидкости
В отличие от газов, жидкости обладают определенным объемом и формой. Молекулы жидкостей находятся ближе друг к другу, чем молекулы газов, и образуют более слабо связанные структуры. За счет этой связи их объемы ограничены, но молекулы все равно свободно двигаются и меняют свое положение в пределах данного объема. Размеры молекул жидкостей уже не такие маленькие, как у газов, и они могут быть сравнимы с размерами молекул органических соединений или приближенными размерами макромолекул.
Понимание сходств и различий в объеме молекул газов и жидкостей является важным шагом в изучении их свойств и поведения. Помимо размеров, формы и движения молекул, другие факторы, такие как температура и давление, также оказывают влияние на объем и свойства этих веществ.
Разница в размерах органических и неорганических молекул
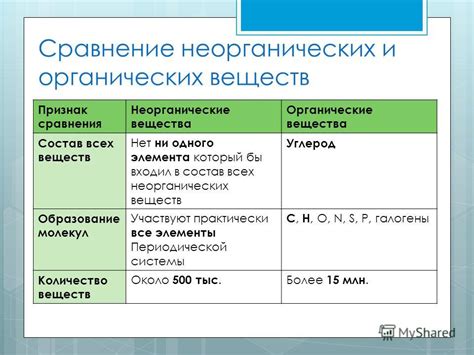
Размер органических молекул зависит от количества и типов атомов, входящих в их состав. Большие органические молекулы могут содержать десятки и сотни атомов, включая углерод, водород, кислород, азот, серу и другие элементы. Благодаря своей сложной структуре, органические молекулы могут образовывать различные связи и принимать разные формы, позволяя им выполнять разнообразные функции в организмах.
В свою очередь, неорганические молекулы, такие как вода, соль и многие другие соединения, обычно состоят из более простых структур и содержат меньшее количество атомов. Их размеры могут быть существенно меньше по сравнению с органическими молекулами. Несмотря на это, неорганические молекулы также выполняют важные функции в природе, обеспечивая поддержание баланса и регулирование химических процессов.
- Размер органических молекул зависит от количества и типов атомов
- Органические молекулы имеют сложную структуру и способны принимать разные формы
- Неорганические молекулы обычно состоят из более простых структур и имеют меньший размер
- Различия в размерах органических и неорганических молекул определяют их функциональные свойства
Гигроскопичность и особенности размеров молекул
Гигроскопичность зависит от химического состава вещества и его структуры. Некоторые материалы обладают высокой гигроскопичностью, поглощая большое количество влаги из окружающей среды и меняя свой объем. Другие, напротив, являются гигроскопически неактивными, то есть не обнаруживают значительных изменений в объеме при контакте с влагой.
Размеры молекул являются неотъемлемой частью химической структуры вещества. Они определяются числом атомов и химической связью между ними. Молекулы разных веществ могут иметь разные формы и размеры: от маленьких и простых, состоящих из двух атомов, до сложных и многоатомных. Размеры молекул напрямую влияют на их взаимодействие с окружающей средой и способность поглощать или отдавать влагу.
Изучение взаимосвязи между гигроскопичностью разных веществ и их молекулярными размерами позволяет лучше понять природу этого явления и применить полученные знания в различных областях, таких как материаловедение, фармацевтика и пищевая промышленность.
Взаимосвязь между поверхностным натяжением и особенностями молекулярной структуры веществ

Исследование влияния поверхностного натяжения на свойства веществ позволяет нам раскрыть интересные особенности структуры и взаимодействия молекул. Поверхностное натяжение возникает из-за сил притяжения между молекулами на поверхности жидкости или при переходе из жидкого в газообразное состояние. Этот феномен определяет поведение вещества и его способность образовывать пленки или капли, а также оказывает влияние на другие характеристики, связанные с молекулярным устройством вещества.
Важно отметить, что величина поверхностного натяжения зависит от химического состава и структуры молекул, а также от условий, при которых происходит измерение. Межмолекулярные силы, такие как ван-дер-ваальсово взаимодействие, диполь-дипольное взаимодействие или водородная связь, играют ключевую роль в формировании сил поверхностного натяжения. Чем сильнее взаимодействие между молекулами вещества, тем выше будет его поверхностное натяжение.
В данном разделе мы рассмотрим различные вещества, исследуя их поверхностное натяжение и анализируя его связь с объемом и состоянием молекул. Ответы на вопросы о сходстве или различии объема молекул в разных веществах можно найти, исследуя влияние поверхностного натяжения на их молекулярную структуру и силы взаимодействия между молекулами.
Важность размеров молекул в химических процессах

Геометрические параметры молекул веществ играют существенную роль во множестве химических реакций. Несмотря на то, что направленность реакций определяется свойствами самой вещества, объем молекул и их взаимное расположение могут влиять на характер реакции и скорость протекания процесса.
Взаимодействие молекул и реакционных частиц зависит от их размеров и формы. Даже малейшее изменение геометрических параметров молекул может привести к различным результатам химических реакций. Например, в некоторых случаях увеличение объема реагента может увеличить скорость реакции, а в других - привести к обратному эффекту.
Важность объема молекул в химических реакциях не ограничивается только скоростью процесса. Он также может влиять на образование продуктов реакции, образование промежуточных соединений и различные физические свойства полученных веществ.
Исследование влияния размеров молекул на протекание химических реакций является важной задачей современной химии. Понимание этого фактора позволяет более точно прогнозировать результаты реакций, разрабатывать новые материалы и оптимизировать условия производства различных веществ.
Роль размера молекул в науке и технологиях
Размер молекул играет ключевую роль в определении многих химических и физических свойств вещества. Молекулы, будучи элементарными частицами, обладают определенным объемом, который влияет на их взаимодействие с другими молекулами и окружающей средой. Размер молекул может быть критичным фактором при проектировании новых материалов с определенными свойствами, такими как прочность, эластичность, проводимость и т.д.
Знание о размере молекул и их взаимодействии помогает ученым разрабатывать новые способы синтеза и модификации материалов, находить применение в различных отраслях науки и технологий. Например, в медицине и фармацевтической промышленности знакомство с размером молекул позволяет разработать новые лекарственные препараты с улучшенной селективностью и эффективностью. В электронике и энергетике понимание размера молекул полезно для создания новых материалов с высокой электропроводностью и эффективности использования энергии.
Вопрос-ответ

Какую роль играет объем молекул в свойствах вещества?
Объем молекул вещества играет важную роль в его физических и химических свойствах. Например, вещества с малыми молекулами, такими как газы, обладают низкой плотностью и могут быть сжатыми легче, чем вещества с большими молекулами, такими как полимеры. Также, объем молекул может влиять на точку кипения и твердость вещества.
Сходятся ли объемы молекул в разных веществах?
Объемы молекул в разных веществах могут сходиться или различаться в зависимости от их химической структуры и взаимодействий между молекулами. Некоторые молекулы имеют схожий размер, независимо от вещества, в котором они находятся, например, молекулы воды. Однако, другие вещества могут иметь молекулы различных размеров и форм, что влияет на их объемы.
Какие факторы могут оказывать влияние на объем молекул вещества?
Объем молекул вещества может зависеть от нескольких факторов. Во-первых, это может быть связано с размером и формой самой молекулы. Например, углеводороды, состоящие из простых линейных цепочек, имеют маленькие и схожие объемы молекул. Во-вторых, влиять на объем молекул может также степень их взаимодействия с окружающими молекулами. Например, молекулы веществ, имеющих силные взаимодействия, могут занимать более компактное пространство, чем молекулы веществ с слабыми взаимодействиями.



