Проникновение в мир молекул позволяет нам осознать величину разнообразия природных объектов и различий между ними. Каждая молекула, будь то простейший атом или сложное органическое соединение, обладает своей уникальной структурой, в каждом элементе которой заключены невероятные силы и свойства. Это как открытие сокровищницы знаний, открывающее перед нами мир непостижимых возможностей. Различия в молекулярной структуре определяют, как вещество будет вести себя в определенных условиях и взаимодействовать с окружающей средой.
Молекулярная симфония природы заставляет нас пересматривать наши представления об окружающем мире. Наблюдая различные явления и процессы, мы можем увидеть, как ритмично и неуклонно работает молекулярный оркестр. Все эти пульсирующие частицы, неуловимые для глаза, тесно связаны и слажено взаимодействуют друг с другом. Гармония молекулярной структуры открывает перед нами интересные паттерны и законы, которые можно применить и в практической деятельности.
Когда мы задаемся вопросом "Почему?" или "Как это работает?", мир молекул отвечает наши ожидания. Каждая молекула, хотя и невидима, содержит в себе ключ к пониманию множества явлений, которые на первый взгляд кажутся неразрешимыми головоломками. Разбираясь с этими загадками, мы раскрываем перед собой новые горизонты знаний и открываем возможности для создания новых материалов и технологий. В исследовании молекулярной структуры лежит ответ на множество вопросов, и это захватывает нас своими неограниченными гранями и перспективами.
Открытие и принципы молекулярной концепции: основа современной науки

В данном разделе мы рассмотрим историческое открытие и фундаментальные принципы молекулярной концепции, которые положили основу для развития современной науки. Молекулярная концепция объясняет различия в свойствах веществ и явлениях, основываясь на микроскопической структуре вещества, состоящей из молекул.
История молекулярной концепции начинается с древних греков, которые предполагали, что все вещества состоят из неделимых частиц, названных атомами. Однако было необходимо дождаться развития научных методов и технологий, чтобы подтвердить эту теорию на практике. | Развитие молекулярной концепции связано с работами таких ученых, как Джон Дальтон, Авогадро, Оствальд, Жан Перрен и другие. Они провели серию экспериментов и разработали математические модели, которые доказали, что вещества состоят из мельчайших частиц, и назвали их молекулами. |
Основные принципы молекулярной концепции включают идею о том, что каждая молекула обладает определенной структурой и связями между атомами. Также важным принципом является представление о том, что различные вещества образуются путем объединения определенных типов атомов в молекулы с определенными комбинациями связей. | Молекулярная концепция объясняет множество явлений, включая физические и химические свойства вещества, состояние агрегации, реакции между веществами и т.д. Понимание молекулярной структуры вещества позволяет ученым проектировать новые материалы и создавать новые технологии. Также это показывает, что наша реальность состоит из невидимых мельчайших частиц, что расширяет наше понимание мира. |
Происхождение концепции молекулярной природы вещества

Изучение природы вещества неизбежно привело к возникновению и развитию молекулярной теории. Ученые старались понять, какие строительные блоки присутствуют в различных веществах и как они связаны между собой. Это предположение формировало основу для дальнейшего развития молекулярной теории, которая объясняет множество различий, наблюдаемых в свойствах веществ.
Одной из ключевых идей, лежащих в основе молекулярной теории, является концепция существования мельчайших частиц материи, называемых молекулами. Версии этой концепции возникали в разных временах и среди разных ученых, но главное объединяющее звено - представление о том, что все вещества состоят из отдельных молекул и их взаимодействий. Эти молекулы, будучи неделимыми и непрерывными, определяют свойства и поведение веществ.
Проблема происхождения молекулярной концепции возникла еще в древние времена, но она начала получать более научное обоснование только в XVII веке. Ученые, такие как Рене Декарт и Пьер Гассент, предполагали, что существуют неделимые частицы, которые объединяются для формирования различных веществ.
Впервые научное обоснование молекулярной концепции получила благодаря работам Джона Далтона и его атомистической теории. Далтон предложил модель, в которой все вещества состоят из отдельных неделимых частиц - атомов, которые соединяются в определенных пропорциях для образования молекул. Эта идея, развиваемая впоследствии учеными, положила основу для дальнейшего исследования и объяснения различных свойств различных веществ.
Основные принципы осмысления молекулярного строения и взаимодействия веществ
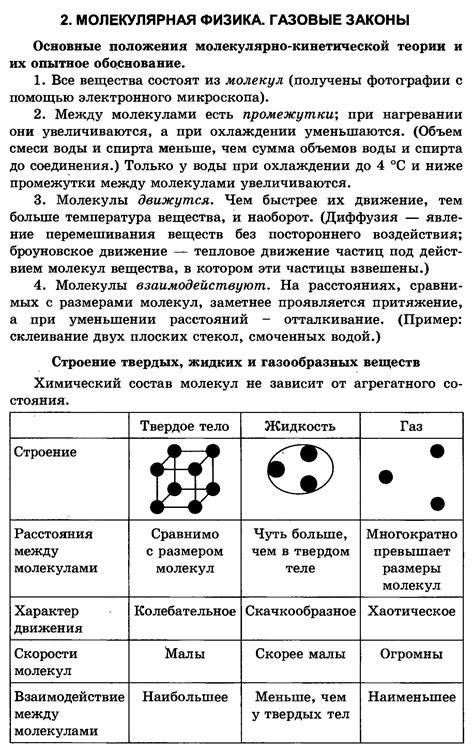
В данном разделе мы рассмотрим основные принципы, которые лежат в основе понимания молекулярного строения и взаимодействия веществ. Будут рассмотрены принципы, позволяющие объяснить различия в свойствах веществ на молекулярном уровне, а также способы анализа и изучения молекулярной структуры.
Одним из ключевых принципов является понятие взаимодействий между атомами и молекулами. Разнообразие свойств веществ обусловлено их уникальной молекулярной организацией, в которой каждый атом или группа атомов занимает свое место и обладает определенными свойствами.
Другим важным принципом является симметрия молекул, которая влияет на их свойства и взаимодействия. Взаимное расположение атомов в молекуле может создавать положительные и отрицательные заряды, что определяет химические свойства вещества.
Также в данном разделе будет представлено понятие связей между атомами и молекулами, которые являются основой для формирования молекулярной структуры. Различные типы связей обладают разными физическими и химическими свойствами, что приводит к разнообразию веществ и их реакций.
Исследование молекулярных структур и их взаимодействий представляет огромную значимость для различных областей науки и технологий. Понимание основных принципов молекулярной теории позволяет не только объяснить различия в свойствах веществ, но и прогнозировать и контролировать их химические и физические процессы.
Взаимосвязь между структурой молекулы и ее уникальными свойствами
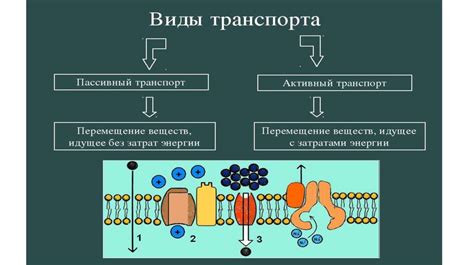
Понимание связи между структурой молекулы и ее свойствами является основой для развития новых материалов, лекарственных препаратов и технологий. Изучение молекулярной структуры вещества позволяет определить его физико-химические характеристики, такие как точка кипения, теплопроводность, плотность и др.
- Молекулярная структура органических соединений и их свойства.
- Молекулярная структура неорганических соединений и их свойства.
- Влияние молекулярной структуры на физико-химические свойства вещества.
- Взаимосвязь между молекулярной структурой и реакционной способностью вещества.
- Применение знаний о молекулярной структуре для создания новых материалов и препаратов.
Изучение молекулярной структуры и свойств вещества играет важную роль в различных областях наук, начиная от химии и физики, и заканчивая медициной и инженерией. Оно позволяет понять, почему некоторые вещества обладают определенными свойствами, а другие - нет, а также открыть новые возможности для создания более эффективных и функциональных материалов.
Влияние организации молекул на физические свойства: взаимосвязь структуры и свойств
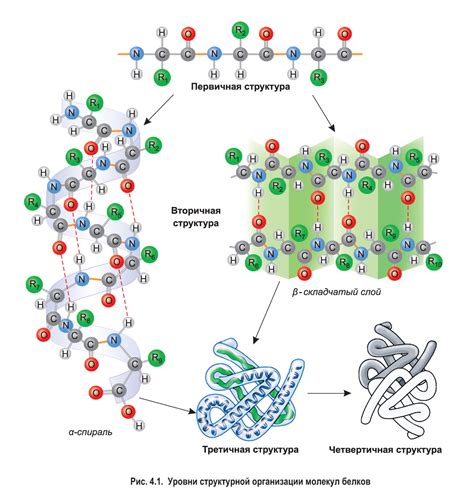
Структура молекулы играет ключевую роль в определении физических свойств вещества. Какие именно свойства и как сильно зависят от молекулярной организации? В данном разделе мы рассмотрим влияние молекулярной структуры на основные физические характеристики веществ.
- Точка плавления и кипения
- Теплоемкость
- Поларность и растворимость
- Плотность и вязкость
- Электрические и оптические свойства
Одно из наиболее очевидных проявлений влияния молекулярной структуры на физические свойства - изменение точки плавления и кипения. Организация молекул вещества определяет, насколько легко оно переходит из твердого состояния в жидкое и газообразное. При более сложной, переплетенной структуре, точка плавления может быть выше, а при простой, линейной структуре - ниже.
Молекулярная организация также влияет на теплоемкость вещества. Более сложная структура делает вещество способным поглощать и отдавать больше тепла без значительного изменения температуры. Таким образом, свойства проводить тепло могут значительно отличаться у различных веществ.
Структура молекулы может определять ее поларность и растворимость. Вещества с поларной структурой имеют проницаемость к электрическим полям и могут взаимодействовать с другими поларными веществами. Такие вещества обычно также легко растворяются в полярных растворителях, в то время как неполярные вещества предпочитают неполярные растворители.
Молекулярная структура влияет на плотность и вязкость вещества. Более компактная структура обычно приводит к повышению плотности. Однако, такая структура также может приводить к повышенной вязкости, потому что молекулы могут сильно взаимодействовать между собой.
Организация молекул в веществе может сильно влиять на его электрические и оптические свойства. Например, вещества с полностью ионизированными молекулами могут пропускать электрический ток, в то время как вещества с неполярными молекулами могут быть электрическими изоляторами. Также, структура и форма молекулы может определять способность вещества поглощать или пропускать свет, что влияет на его оптические свойства.
Таким образом, понимание и анализ молекулярной структуры вещества позволяет лучше понять его физические свойства и явления. В следующих разделах мы более подробно рассмотрим каждое из физических свойств вещества в контексте его молекулярной структуры.
Химические свойства веществ и их связь с устройством молекулярной структуры
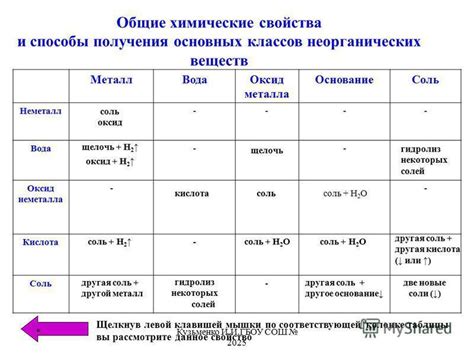
В данном разделе мы рассмотрим взаимосвязь между химическими свойствами веществ и их молекулярной структурой. В мире химии существует огромное разнообразие веществ, каждое из которых обладает своими уникальными свойствами. Эти свойства определяются не только типом атомов, но и способом, которым эти атомы организованы в молекуле.
Молекулярная структура вещества может быть сложной и разнообразной. Она описывает пространственное расположение атомов и связей между ними. Взаимосвязь между молекулярной структурой и химическими свойствами веществ имеет особое значение для понимания и объяснения разнообразных явлений, таких как реакции, фазовые переходы и возникновение новых веществ.
| Химическое свойство | Связь с молекулярной структурой |
|---|---|
| Реакционная активность | Молекулярная структура определяет наличие и доступность активных центров, которые участвуют в химических превращениях. |
| Растворимость | Молекулярное строение вещества влияет на взаимодействие его молекул с растворителем и, следовательно, на его способность растворяться. |
| Термическая стабильность | Молекулярная структура может обуславливать стабильность вещества при нагревании и его способность выдерживать высокие температуры. |
| Электропроводность | Наличие или отсутствие свободных электронов в молекулярной структуре влияет на электропроводность вещества. |
Это лишь некоторые примеры взаимосвязи между молекулярной структурой и химическими свойствами веществ. Понимание этой связи позволяет не только объяснить множество явлений, но и создавать новые вещества с определенными свойствами, которые могут быть применены в разных сферах науки и технологии.
Вопрос-ответ

Как молекулярная теория объясняет различия между разными веществами?
Молекулярная теория позволяет понять, что различия между веществами заключаются в их молекулярной структуре. Каждое вещество состоит из определенного типа молекул, которые могут быть разного размера, формы и состоять из разных атомов. Эти различия в молекулярной структуре определяют химические и физические свойства вещества, такие как температура плавления и кипения, плотность, растворимость и т.д.
Какие факторы могут влиять на молекулярную структуру вещества?
Молекулярная структура вещества зависит от нескольких факторов. Во-первых, химический состав вещества, то есть типы и количество атомов, из которых состоят молекулы. Во-вторых, способ, которым атомы соединены друг с другом, определяет форму и размер молекулы. Например, молекулы веществ могут быть линейными, ветвистыми или кольцевыми. Третий фактор - взаимодействия между молекулами, такие как водородные связи или взаимодействия Ван-дер-Ваальса. Все эти факторы влияют на физические и химические свойства вещества.
Может ли изменение молекулярной структуры вещества привести к изменению его свойств?
Да, изменение молекулярной структуры вещества может привести к изменению его свойств. Например, если изменить способ, которым молекулы соединены, можно изменить температуру плавления и кипения вещества или его растворимость. Также изменение химического состава вещества может привести к изменению его химических свойств, таких как реакционная активность или способность образования новых соединений. Поэтому молекулярная структура играет ключевую роль в определении свойств вещества.



