В мире химии существует множество веществ, которые участвуют в различных реакциях и процессах. При изучении свойств веществ и их взаимодействия, одной из важнейших характеристик является массовая доля. Она представляет собой меру присутствия конкретного компонента в смеси или растворе. Независимо от того, является ли речь о химических реакциях, производстве материалов, фармацевтике или пищевой промышленности, массовая доля вещества играет решающую роль в определении свойств и качества продукта.
Суть понятия массовой доли заключается в том, что она описывает, насколько велик вклад определенного вещества в общую массу смеси или раствора. Таким образом, массовая доля позволяет определить количественные соотношения компонентов и, следовательно, предсказать химическую активность, физические свойства и взаимодействия с другими веществами.
Однако, для точных и надежных результатов измерения массовой доли вещества необходимо учитывать несколько влияющих факторов. Во-первых, важную роль играет метод анализа и измерения. Разные методы могут давать различные результаты, поэтому выбор методики должен быть обоснован научно и требует внимания к деталям. Во-вторых, необходимо учитывать условия смешивания и хранения веществ, так как они могут влиять на равномерность распределения компонентов и, следовательно, на массовую долю.
Определение и измерение концентрации вещества в растворе: понятие и методы

Для определения массовой доли вещества в растворе существует несколько методов. Один из них основан на использовании аналитических весов для точного измерения массы вещества и общей массы раствора. Другой метод основан на использовании физических свойств раствора, например, плотности или линейного расширения, чтобы вычислить массу вещества.
Стоит отметить, что массовая доля вещества в растворе может быть влияна различными факторами, такими как температура, давление, концентрация других веществ, а также химические реакции и взаимодействия между компонентами раствора.
Измерение массовой доли вещества в растворе является важным шагом в практических исследованиях и промышленных процессах. Корректное определение концентрации вещества позволяет предсказывать и контролировать химические реакции, разрабатывать оптимальные условия хранения и транспортировки растворов, а также оптимизировать производство и применение различных продуктов и материалов.
Роль массовой доли в химии: главное понятие и его значимость

Массовая доля выражает отношение массы данного компонента к общей массе системы и измеряется в процентах, долях или граммах. Она является важным показателем, позволяющим определить концентрацию вещества в смеси и оценить его конкурентоспособность в химических процессах. Также массовая доля может влиять на физические и химические свойства вещества, его степень растворимости и способность реагировать с другими веществами.
Понимание и учет массовой доли в химии позволяет проводить точные расчеты и дозировки при синтезе новых соединений, анализе растворов и контроле качества продукции. Кроме того, понятие массовой доли особенно важно в области экологии и безопасности, так как дает возможность оценить загрязненность водных и воздушных сред, а также разрабатывать эффективные методы очистки и дезинфекции.
Измерение содержания вещества в растворе: методы и принципы

При изучении массовой доли вещества в растворе, наши представления о его содержании влияют на различные факторы и играют важную роль в практических приложениях. Понимание способов, с помощью которых можно измерить содержание вещества, становится незаменимым в определении концентрации и контроле качества в различных отраслях науки и промышленности.
При определении массовой доли вещества в растворе применяются различные методы и принципы. Один из наиболее распространенных методов - гравиметрический, основанный на измерении массы с образцом. Другим методом является волюметрия, основанная на измерении объема раствора, взаимодействие которого с определенным реагентом известно. Кроме того, вещество может быть измерено с использованием спектрофотометрии, где его концентрация определяется путем анализа поглощения света при определенной длине волны.
Также существуют методы, основанные на физических свойствах веществ, таких как плотность или температура кипения. Эти методы позволяют измерять концентрацию вещества с помощью инструментов и приборов, специально разработанных для таких измерений.
Правильный выбор метода измерения массовой доли вещества в растворе зависит от его химических свойств, концентрации вещества и доступных инструментов. Критическое понимание принципов и ограничений каждого метода позволяет получить точные и репрезентативные результаты и является ключевым в ведении аналитической работы в различных областях науки и промышленности.
Воздействующие факторы на пропорцию веществ в растворе

Во-первых, условия смешивания важно учитывать при анализе массовой доли вещества в растворе. Интенсивность перемешивания и время, затраченное на смешивание, могут сильно повлиять на равномерность распределения компонентов в растворе. Недостаточное перемешивание может вызвать неравномерную распределение вещества и, как следствие, искажение массовой доли.
Во-вторых, растворимость вещества в растворителе также определяет его массовую долю в растворе. Исключительная растворимость может привести к высоким концентрациям вещества, тогда как низкая растворимость может привести к низкой массовой доле.
Также, температура раствора играет важную роль. Увеличение температуры может способствовать повышению растворимости и, следовательно, увеличению массовой доли вещества в растворе. Однако, есть случаи, когда повышение температуры может вызвать обратный эффект и привести к снижению массовой доли вещества.
Концентрация вещества в растворе также оказывает значительное влияние на его массовую долю. Чем выше концентрация, тем больше массовая доля вещества. Давление также может влиять на массовую долю, особенно в случаях, когда раствор обладает газообразным компонентом.
Таким образом, понимание всех этих факторов, которые влияют на массовую долю вещества в растворе, является важной основой для анализа и понимания состава различных растворов. Эти факторы должны быть учтены и приняты во внимание при проведении экспериментов и исследований, связанных с составом растворов.
Растворимость и значимость в оценке количества вещества
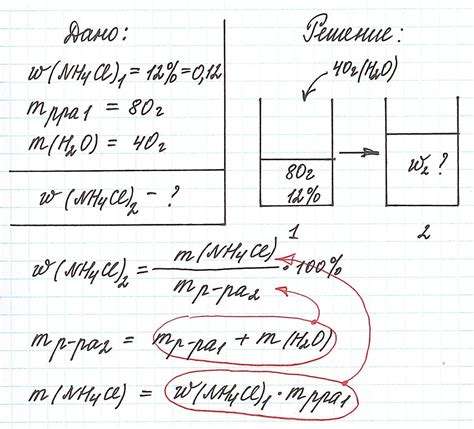
В процессе изучения массовой доли вещества в растворе невозможно обойти тему растворимости и ее важность в определении данного показателя. Растворимость представляет собой способность вещества растворяться в другом веществе при заданных условиях. Она может быть определена исходя из различных факторов, таких как температура, давление и химические свойства соединения, а также распределение кислорода или других ионов в водной среде.
Роль растворимости в определении массовой доли состоит в том, что она помогает установить количество вещества, содержащегося в растворе, с учетом его массы и концентрации. При изучении этого показателя необходимо учитывать, что разные вещества обладают разной степенью растворимости, и это может существенно влиять на результаты исследования. Например, нерастворимые вещества могут быть исключены из расчетов, а растворимые – учтены при определении массовой доли их компонентов.
Таким образом, понимание растворимости и ее роли в определении массовой доли является ключевым при изучении данной темы. Различные факторы, влияющие на растворимость, нужно учитывать и анализировать при оценке количества вещества на основе массовой доли. Это позволяет получать более точные и достоверные результаты исследований, а также применять полученные знания в различных областях науки и промышленности.
Влияние температуры и давления на содержание вещества в растворе
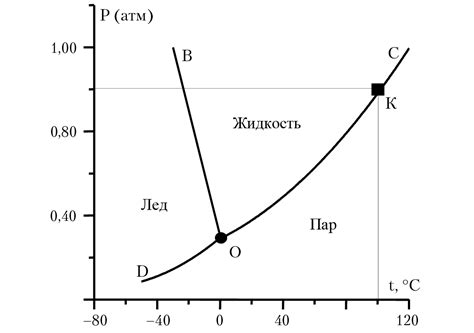
Физические параметры, такие как температура и давление, играют важную роль в определении содержания определенного вещества в растворе. Изменения в этих факторах могут вызвать значительное изменение массовой концентрации в растворе.
Температура влияет на растворимость вещества, то есть на его способность таиться в растворе. Повышение температуры может привести к увеличению растворимости, в то время как понижение температуры может вызвать обратный эффект. Это объясняется изменениями в молекулярной активности и энергии, что ведет к изменению числа частиц в растворе.
Давление также может оказывать влияние на массовую концентрацию вещества в растворе. Когда давление повышается, объем растворителя может уменьшаться, что приводит к увеличению концентрации вещества. Это наблюдается в особенности при растворении газовых веществ, где давление играет важную роль в обратимости процесса.
Взаимодействие компонентов смеси и его влияние на содержание вещества
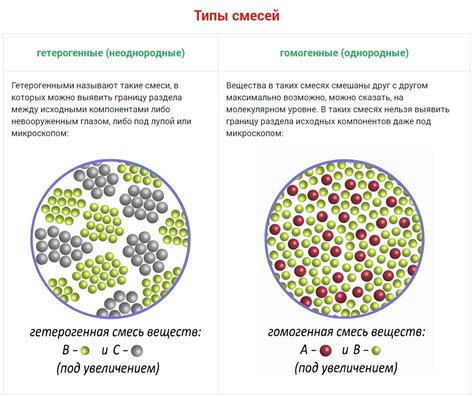
В данном разделе мы рассмотрим взаимодействие различных компонентов, присутствующих в растворе, и его влияние на содержание конкретного вещества. Компоненты смеси могут проявлять различные свойства, взаимодействуя между собой и влияя на процесс образования раствора.
При взаимодействии компонентов могут происходить различные химические и физические процессы, такие как образование новых соединений, образование комплексов, сорбция, коагуляция и другие. Эти процессы могут оказывать существенное влияние на распределение и концентрацию составляющих веществ в растворе.
Одним из ключевых факторов, определяющих массовую долю конкретного вещества, является его растворимость в данной смеси. Растворимость зависит от взаимодействия между молекулами вещества и молекулами растворителя, а также от условий среды, таких как температура и давление. Изменение одного из этих параметров может привести к изменению растворимости и, следовательно, к изменению массовой доли вещества в растворе.
Кроме того, некоторые компоненты могут проявлять способность взаимодействовать между собой и образовывать ассоциаты или соединения с более низкой растворимостью. Это также может влиять на массовую долю вещества в растворе и приводить к образованию отдельных фаз или осаждению вещества.
Взаимодействие компонентов раствора и их влияние на массовую долю вещества представляет собой сложный и многоаспектный процесс, требующий учета различных факторов и свойств компонентов. Понимание этих взаимодействий позволяет более точно определить и контролировать массовую долю вещества в растворе, что имеет важное значение во многих областях науки и промышленности.
| Взаимодействие компонентов | Влияние на массовую долю вещества |
|---|---|
| Химические реакции | Образование новых соединений с изменением содержания вещества |
| Физические процессы | Процессы сорбции, коагуляции и другие, которые могут привести к изменению массовой доли вещества |
| Растворимость | Влияние взаимодействия молекул растворителя и вещества на массовую долю |
| Образование ассоциатов | Возможность образования комплексов с более низкой растворимостью, что может привести к образованию отдельных фаз |
Вопрос-ответ

Что такое массовая доля вещества в растворе?
Массовая доля вещества в растворе – это количество вещества, выраженное в граммах, содержащееся в данном растворе на единицу его массы, выраженной также в граммах. Определяется она как отношение массы растворенного вещества к массе всего раствора и умножается на 100 для получения процентного значения.
Как определить массовую долю вещества в растворе?
Для определения массовой доли вещества в растворе необходимо знать массу растворенного вещества и массу всего раствора. Масса растворенного вещества делится на массу всего раствора, а затем результат умножается на 100. Таким образом, получается массовая доля вещества в растворе в процентном выражении.
Какие факторы могут влиять на массовую долю вещества в растворе?
Массовая доля вещества в растворах может быть подвержена влиянию различных факторов. Некоторые из них включают: количество растворенного вещества, массу распорядительной жидкости или раствора, способ смешивания, температуру, давление и концентрацию реагентов. Все эти факторы могут влиять на итоговую массовую долю вещества в растворе.
Можно ли изменить массовую долю вещества в растворе?
Да, массовую долю вещества в растворе можно изменить. Это можно сделать путем добавления или удаления реагентов, изменения температуры, давления или концентрации реагентов, а также с помощью различных методов смешивания. Изменение этих параметров может привести к изменению массовой доли вещества в растворе.



