Замыкающие в себе испепеляющие лучи солнца, растворяться вонзаются в густую ткань воздуха, путешествуют в огромной концентрации. Они исхудали и истончились от постоянного столкновения со своими собратьями, а их точность и непосредственность неоспоримы. Помните, теория Больцмана утверждает, что все структуры тесно связаны друг с другом, образуя движение постоянного танца. Это движение молекул является одной из фундаментальных основ физики, определяющей обработку этой системы.
Однако, несмотря на свою микроскопическую размерность, молекулы обладают неотъемлемыми свойствами - объемом и давлением, которые позволяют определить их количество в данной системе. Исходя из этого факта, встает вопрос о том, каким образом можно установить число молекул, исходя из известных параметров объема и давления.
Разные научные группы на протяжении долгих лет пытались разработать простой и эффективный метод, позволяющий решать эту задачу. Некоторые предлагали использовать сложные модели и уравнения, требующие больших вычислительных мощностей и обширных исходных данных. Другие, нацеленные на простоту и доступность метода, обосновывали свои решения на основе упрощенных моделей и экспериментальных данных.
Основы определения количества частиц: ключевые принципы и стратегии

В этом разделе мы рассмотрим основные принципы и стратегии для определения количества частиц в физической системе. Мы изучим фундаментальные понятия, связанные с определением количества молекул, атомов или ионов, без использования прямых измерений, основанных на объеме и давлении физической системы. Эти подходы позволяют получить достоверные результаты, используя разнообразные методы анализа и расчета.
Физические принципы, лежащие в основе расчета количества молекул

Расчет числа молекул в физике основан на нескольких физических законах, которые позволяют определить связь между объемом, давлением и количеством молекул в газе. Используя эти законы, можно получить точные значения количества частиц, находящихся в заданном объеме при определенном давлении.
Один из таких законов - это идеальный газовый закон, который описывает поведение идеальных газов и позволяет установить зависимость между их объемом, давлением и температурой. Кроме того, закон Клапейрона-Менделеева описывает связь между объемом газа и его температурой при неизменном количестве молекул. Эти законы позволяют установить основные принципы расчета количества молекул по заданным параметрам.
Для более точного расчета используется также понятие молярной массы, которая определяет массу одной молекулы вещества относительно молярного веса. Это позволяет учесть различия в массе молекул разных веществ и получить более точные значения.
| Физический закон | Описание |
|---|---|
| Идеальный газовый закон | Описывает связь между объемом, давлением и температурой идеальных газов. |
| Закон Клапейрона-Менделеева | Описывает связь между объемом газа и его температурой при неизменном количестве молекул. |
| Молярная масса | Определяет массу одной молекулы вещества и учитывает различия массы молекул разных веществ. |
Эти физические принципы являются основой для расчета числа молекул в физике. Используя данные о объеме и давлении газа, можно применить соответствующие законы и определить точное количество молекул в заданном объеме при заданном давлении. Этот метод является надежным и эффективным способом расчета, который находит применение в различных областях физики и химии.
Определение объема и давления: ключевые понятия

Определение объема представляет собой процесс измерения пространства, заполненного определенной субстанцией или газом. Объем может быть выражен в разных единицах измерения, таких как литры, кубические метры или галлоны. Он является ключевым параметром для понимания физических свойств вещества.
Давление, с другой стороны, определяется как сила, действующая на единицу площади. Оно является результатом столкновения и взаимодействия молекул вещества. Давление играет важную роль в понимании различных процессов в физике, таких как сжатие и расширение газов, а также изменение состояния вещества.
Понимание и изучение объема и давления помогает нам лучше понять молекулярную структуру вещества и предсказывать его физические свойства. Комбинируя знания о объеме и давлении, мы сможем более эффективно определять количество молекул в физической системе.
- Объем - основной параметр в измерении свойств вещества
- Давление - результат столкновения и взаимодействия молекул
- Определение объема и давления - ключевые шаги для понимания физических процессов
- Изучение объема и давления помогает понять молекулярную структуру вещества
Уравнение состояния и идеальный газ: взаимосвязь с количеством частиц
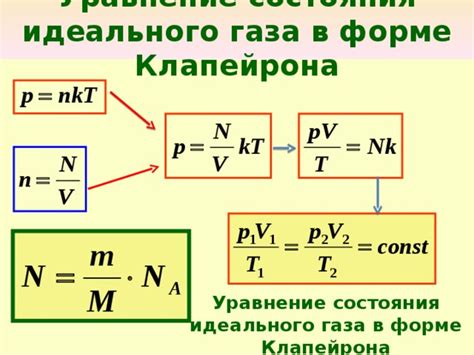
В данном разделе мы рассмотрим связь между уравнением состояния и идеальным газом с количеством частиц в системе. Определение состояния газа включает в себя его объем и давление, а также количество молекул, которые находятся в этом объеме и взаимодействуют друг с другом.
Уравнение состояния газа описывает зависимость между давлением, объемом и температурой газа. В случае идеального газа, который является упрощенной моделью реального газа, это уравнение есть линейная связь между этими величинами.
Однако, чтобы полностью описать состояние газа, необходимо также учитывать количество молекул, которые находятся в данном объеме. Количество молекул влияет на величину давления и объема, так как каждая молекула взаимодействует с другими молекулами и совершает столкновения со стенками сосуда.
Для учета количества молекул в системе существует понятие молярной массы идеального газа, которая обозначается как масса одной молекулы, умноженная на количество молекул в данной системе. Молярная масса позволяет связать количество молекул с массой газа и его плотностью.
| Физическая величина | Обозначение | Описание |
|---|---|---|
| Давление | P | Сила, действующая на единицу площади |
| Объем | V | Пространство, занимаемое газом |
| Температура | T | Мера средней кинетической энергии частиц |
| Количество молекул | N | Число частиц в газе |
| Молярная масса | M | Масса одной молекулы, умноженная на количество молекул |
Расчет количества молекул через объем и давление: простой путь к ответу

Исследование физических систем требует умения определить количество молекул в данном объеме при заданном давлении. Хотя этот процесс может показаться сложным и эффективным, существует простой метод, позволяющий легко решить данную задачу.
Сущность связи между количеством частиц и объемом в физике: интуитивное понимание
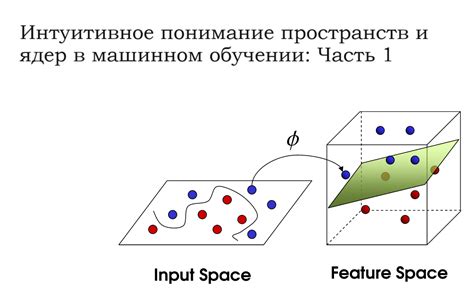
Интуитивное понимание этой связи позволяет нам представить, как увеличение объема может привести к увеличению числа молекул. Когда мы увеличиваем объем, мы предоставляем больше места для молекул, что может привести к повышению их числа.
Представьте себе контейнер, наполненный небольшими шариками. Если увеличить объем контейнера, добавив в него больше шариков, то общее число шариков в контейнере возрастет. Так же происходит и с молекулами или атомами в объеме.
Например, если мы приложим силу и расширим резиновый шар, содержащий внутри молекулы газа, мы увеличим его объем. При этом количество молекул внутри шара останется неизменным, так как мы не добавляем новые молекулы, а просто расширяем пространство, в котором они находятся.
Важно отметить, что связь между числом молекул и объемом является взаимосвязанной и зависит от других факторов, таких как давление и температура. Понимание этой связи позволяет нам лучше осознать, как изменения в объеме влияют на количество молекул в системе, и в свою очередь, на общие физические свойства вещества.
Расчет количества частиц по уравнению состояния идеального газа

В данном разделе рассматривается методика определения числа молекул идеального газа на основе уравнения состояния. Используя концепцию идеального газа, возможно вычислить количество частиц, основываясь на известных величинах объема и давления.
Уравнение состояния идеального газа является основой для расчетов. Оно устанавливает связь между давлением, объемом и температурой газа. Пользуясь этим уравнением, можно определить количество молекул или атомов в данной системе.
- Шаг 1: Запишите уравнение состояния идеального газа с известными величинами давления и объема.
- Шаг 2: Выразите неизвестную величину - количество частиц газа.
- Шаг 3: Подставьте известные значения давления и объема в уравнение и решите его, чтобы получить искомую величину.
Таким образом, применение уравнения состояния идеального газа позволяет определить количество молекул газа и изучить его структуру, основываясь на объеме и давлении системы.
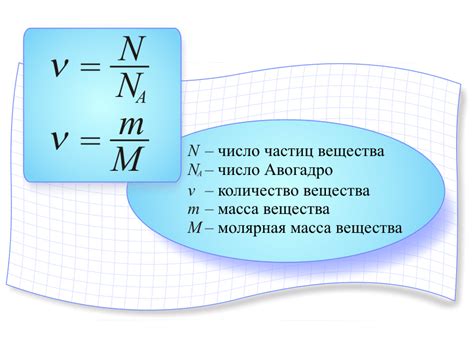
Применение закона Авогадро в определении количества молекул
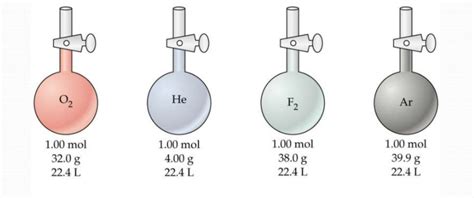
- Введение в закон Авогадро
- Описание количества вещества
- Связь между количеством вещества и числом молекул
- Молярный объем и его значение
- Применение закона Авогадро в расчетах
- Примеры применения закона Авогадро
- Ограничения и пределы применения закона Авогадро
Понимание закона Авогадро является важным для определения количества молекул в системе с использованием объема и давления. Раздел приведет несколько примеров, иллюстрирующих практическое применение закона Авогадро и поможет читателю получить представление о количестве молекул в системе на основе этих параметров. Однако стоит отметить, что применение закона Авогадро имеет свои пределы и ограничения, которые также будут рассмотрены в данном разделе.
Влияние температуры на определение количества молекул в системе
При изучении количества молекул в системе, учитывание температуры позволяет ученным получать более точные и надежные результаты. Изменение температуры влияет на скорость движения молекул и их энергию. Это в свою очередь влияет на объем и давление, которые используются для определения количества молекул в системе.
| Температура | Влияние на движение молекул | Влияние на энергию молекул |
|---|---|---|
| Низкая | Медленное движение молекул | Малая энергия молекул |
| Высокая | Быстрое движение молекул | Высокая энергия молекул |
Таким образом, зная температуру системы, ученые могут учитывать влияние температуры на движение и энергию молекул для более точного определения количества молекул в системе на основе объема и давления.
Применение вычислительных методов для определения числа молекул

В данном разделе рассмотрены эффективные приложения вычислительных методов для определения количества молекул в системе. При использовании данных методов, построенных на моделировании и анализе взаимодействий молекул, можно получить более точные результаты, отражающие реальное количество молекул в исследуемой системе.
Одним из применяемых методов является молекулярная динамика, которая позволяет моделировать движение молекул в трехмерном пространстве и анализировать их взаимодействия. Используя этот метод, можно оценить количество молекул в системе на основе числа столкновений и изменения их энергии.
Другим эффективным методом является метод Монте-Карло, который основан на вероятностных вычислениях и случайных выборках. С помощью этого метода можно смоделировать различные состояния системы и симулировать статистическое поведение молекул. После выполнения большого количества итераций можно определить вероятность наличия определенного количества молекул в системе.
| Применение метода | Описание |
|---|---|
| Молекулярная динамика | Моделирование движения молекул и анализ их взаимодействий |
| Метод Монте-Карло | Вероятностные вычисления и симуляции статистического поведения молекул |
Использование данных методов позволяет получить более точные и достоверные результаты определения числа молекул в исследуемой системе. Комбинирование молекулярной динамики с методом Монте-Карло или другими подходами может улучшить точность и эффективность определения количества молекул, что имеет важное значение для различных научных и инженерных задач.
Вопрос-ответ

Каким образом можно определить число молекул в физике по объему и давлению?
Существует несколько методов для определения числа молекул по объему и давлению. Одним из простых и эффективных методов является использование уравнения состояния идеального газа. Для этого необходимо знать значение универсальной газовой постоянной, объем газа и давление. По формуле N = (PV)/(RT), где N - число молекул, P - давление, V - объем, R - универсальная газовая постоянная и T - температура, можно найти количество молекул в газе.
Как определить универсальную газовую постоянную, используя объем и давление?
Универсальная газовая постоянная является физической константой и имеет значение 8.314 Дж/(моль*К). Она определяется экспериментально и используется в уравнении состояния идеального газа. Для определения универсальной газовой постоянной по объему и давлению необходимо воспользоваться следующим выражением: R = (PV)/(NT), где R - универсальная газовая постоянная, P - давление, V - объем, N - количество молей газа и T - температура.
Как можно использовать метод определения числа молекул по объему и давлению в практических задачах?
Метод определения числа молекул по объему и давлению является широко применяемым в практических задачах. Например, в химии этот метод помогает определить количество вещества, если известны объем и давление газа. В физике он может быть использован для расчета числа молекул воздуха в определенном объеме или для определения числа молекул в газовой смеси. Он позволяет получить важные данные для проведения экспериментов и научных исследований.
Как точно можно определить число молекул в физике по объему и давлению?
Точное определение числа молекул в физике по объему и давлению возможно только в идеальных условиях, когда газ полностью соответствует уравнению состояния идеального газа. Однако, в реальных условиях количество молекул может изменяться под влиянием различных факторов, таких как температура, взаимодействия между молекулами и давление. Поэтому найти точное значение числа молекул в физике по объему и давлению достаточно сложно. Однако, используя уравнение состояния идеального газа, можно получить достаточно точные приближенные значения.



