Одним из уникальных свойств химических элементов является их способность менять свою степень окисления в различных реакциях. Это явление играет ключевую роль в многообразии химических процессов, позволяя нам понять и объяснить различные явления, происходящие в природе и технике.
Вместе с пониманием степени окисления элементов их способности и взаимодействовать между собой, мы начинаем понимать сложные превращения веществ, возможности химического синтеза и разложения. В мире элементов можно отыскать настоящие <<химические пазлы>>, где обнаруживается скрытая глубина взаимодействий и возможности природы.
Химическая таблица элементов Менделеева стала основой для открытия и классификации окислительно-восстановительных свойств химических веществ. Взглянув на ее символическую нотацию, мы можем увидеть формулу для полноценной работы с элементами. В ней закодировано понимание, что степень окисления каждого элемента является индивидуальным и характерным свойством.
Идентификация степени окисления в периодической системе элементов
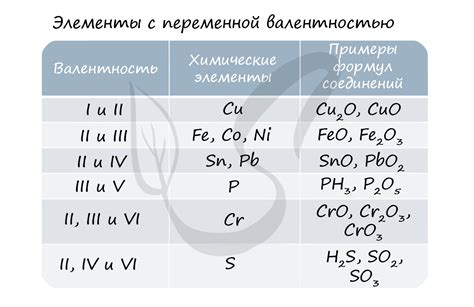
Определение степени окисления
Степень окисления - это числовое значение, которое показывает относительную переходность электронов в химической реакции. Каждому химическому элементу, представленному в периодической системе, сопоставляется определенная степень окисления, которая представляет собой количество электронов, которые элемент способен принять или отдать в реакции.
Важно отметить, что степень окисления может быть положительной (когда элемент теряет электроны) или отрицательной (когда элемент получает электроны). Она может быть целочисленной или нецелочисленной, в зависимости от сложности реакции и переходности электронов.
Определение степени окисления в периодической системе элементов может производиться с использованием различных методов и правил, таких как правило оксианиона, правило нулевой суммы или правило электроотрицательности элементов. Зная степень окисления элементов в соединениях, можно проводить анализ химических реакций, изучать взаимодействия элементов и понимать механизмы химических процессов.
Структура таблицы химических элементов

Рассмотрим структуру таблицы, которая содержит информацию о химических элементах. В этой таблице представлены свойства и характеристики элементов, такие как электронная конфигурация, атомная масса и элементарный состав.
- Первая строка таблицы содержит названия столбцов, которые группируют элементы по их химическим свойствам. Некоторые из этих групп включают щелочные металлы, галогены и инертные газы.
- В каждой строке таблицы указаны различные элементы. Они располагаются по порядку возрастания их атомных номеров. Каждый элемент имеет уникальный символ, который отображается в ячейке таблицы.
- Продолжая вниз по таблице, на других строках представлены дополнительные данные и характеристики элементов. Например, атомная масса и электронная конфигурация, которая описывает количество электронов в каждом атоме элемента.
- Таблица имеет также другие элементы, которые предоставляют дополнительную информацию, такую как номер группы и периода элемента. Эти дополнительные данные расположены в специальных ячейках таблицы.
Все эти элементы в таблице химических элементов совместно помогают исследователям и ученым классифицировать и изучать различные свойства и характеристики химических элементов. Эта таблица является основным инструментом для определения структуры и взаимодействия различных элементов в химических процессах и реакциях.
Поиск информации о окислительном состоянии элементов в таблице

Когда мы изучаем различные химические реакции и даже просто хотим понять, какие вещества могут образоваться в результате взаимодействия различных веществ, знание степени окисления элементов является важным аспектом. Это позволяет нам определить, какие ионы образуются во время реакции, а также предсказать химические свойства соединений.
С помощью таблицы элементов мы можем найти информацию о степенях окисления элементов, такую как число электронов, которые элемент приобретает при образовании ионов. Это дает нам понимание, какие ионы будут образовываться в различных химических реакциях.
Существует несколько способов определения степени окисления элементов в таблице. Один из них - это нахождение номера элемента в таблице и поиск соответствующей информации о его окислительном состоянии. Другой метод - использование заряда иона или ионов, образуемого элементом, для определения его степени окисления.
Таблица элементов представляет собой удобный справочник, который поможет нам быстро определить степень окисления элементов в различных химических соединениях. Знание степени окисления элемента позволяет нам лучше понять его свойства и реакционную способность, что является неотъемлемой частью изучения химии.
В следующих разделах мы рассмотрим более подробно, как найти информацию о степени окисления элементов в таблице и как это знание помогает в химических расчетах и предсказывании химических реакций.
Примеры решения задач по определению окислительно-восстановительной активности различных веществ
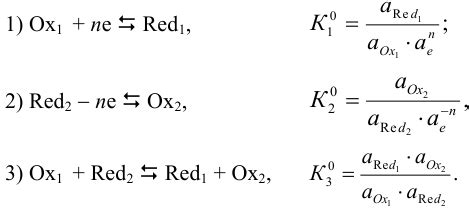
В этом разделе мы представим несколько примеров задач, связанных с определением окислительно-восстановительной активности различных веществ. Определение степени окисления важно с точки зрения химических реакций и взаимодействия разных веществ, а также для понимания их свойств и применения в различных областях.
Первый пример - определение окислительно-восстановительной активности железа в присутствии различных кислот. Мы рассмотрим реакцию между железом и соляной кислотой, исследуем степень окисления железа в этой реакции, а также изучим влияние различных условий на процесс окисления и восстановления.
Второй пример - определение окислительно-восстановительной активности пероксида водорода в присутствии различных катализаторов. Мы изучим, как разные вещества могут повысить или замедлить скорость окисления пероксида водорода, и обсудим влияние концентрации катализатора на реакцию. Также рассмотрим применение этой реакции в аналитической химии для определения концентрации пероксида водорода в пробе.
Третий пример - определение окислительно-восстановительной активности органических соединений. Мы рассмотрим реакции различных органических веществ с окислителями и восстановителями, исследуем изменение состояния этих веществ и определим их степень окисления. Будем изучать влияние разных функциональных групп на свойства и активность органических соединений.
Вопрос-ответ

Как найти степень окисления элемента из таблицы?
Для того чтобы найти степень окисления элемента из таблицы, необходимо знать его положение в периодической системе. Степень окисления определяется по числу электронов, которые элемент принимает или отдает при образовании химических соединений. В таблице элементов можно найти информацию о язычной способности каждого элемента, а также о его электронной конфигурации, что поможет определить степень окисления.
Где найти таблицу элементов для определения степени окисления?
Таблица элементов, включающая периодическую систему, можно найти в учебниках по химии, а также в интернете на различных сайтах. Одним из распространенных источников информации является таблица Д.И. Менделеева. Она содержит данные о всех известных элементах и их химических свойствах, включая степень окисления.
Как определить степень окисления элемента без таблицы?
Если у вас нет таблицы элементов под рукой, то степень окисления можно определить, анализируя химическую формулу соединения, в котором присутствует данный элемент. Для этого необходимо знать правила определения степени окисления, например, веществ с неизменной степенью окисления, окислителей и восстановителей. Также полезно знать общепринятые степени окислений некоторых элементов.
Может ли степень окисления элемента меняться в различных соединениях?
Да, степень окисления элемента может меняться в различных соединениях. Она зависит от того, с какими элементами элемент образует химическое соединение. Например, у железа в соединении FeO его степень окисления равна +2, а в соединении Fe2O3 – +3. Именно по этой причине для определения степени окисления важно знать состав и химическую формулу соединения.
Какие элементы обычно имеют постоянную степень окисления?
Некоторые элементы имеют постоянную степень окисления в большинстве соединений. Например, кислород обычно имеет степень окисления -2, водород – +1, алкалий и щелочноземельные металлы – +1 и +2 соответственно. Эти значения степени окисления следует запомнить, так как они встречаются очень часто в химических реакциях и формулах соединений.
Какие элементы существуют в таблице элементов?
В таблице элементов приведены все известные химические элементы. Всего в таблице представлено 118 элементов, от водорода (H) до оганессона (Og).