Когда мы наблюдаем мир вокруг себя, мы видим различные формы материи - от газообразных облаков до твердых камней. Но что определяет эти различия и почему вещества могут находиться в разных агрегатных состояниях? В физике 8 класса мы начнем изучать основные принципы агрегатного состояния вещества и расширят наши знания о свойствах материи.
Одно из первых понятий, с которыми мы сталкиваемся при изучении физики, - это измерение температуры. Температура играет важную роль в определении состояния вещества. Также важно понимать, что наше восприятие "холодно" и "горячо" может оказаться несоответствующим термическим явлениям, и измерение температуры помогает нам установить четкую шкалу значений.
Когда вещество находится в твердом агрегатном состоянии, его молекулы тесно упакованы и имеют относительно низкую энергию. Это позволяет им сохранять свою форму и объем, и вещества в твердом состоянии обычно обладают определенной прочностью и жесткостью. Если повысить температуру, молекулы начинают вибрировать быстрее и ослабляют свои связи, что приводит к переходу вещества в жидкое состояние.
Основные понятия состояния вещества: ключевые термины и их значения
Молекулы - это частицы, из которых состоят все вещества. Они объединяются вместе, образуя атомы, которые в свою очередь образуют молекулы. Молекулы могут быть разных размеров и форм, в зависимости от вещества, к которому они принадлежат.
Энергия - это сила, которая позволяет молекулам двигаться. В зависимости от количества энергии, молекулы могут двигаться быстро или медленно, а также связываться и разрываться между собой.
Притяжение - это сила, которая держит молекулы вместе. В зависимости от вида вещества, притяжение между молекулами может быть слабым или сильным. Более сильное притяжение между молекулами обычно характерно для твердых веществ, а менее сильное - для жидких и газообразных веществ.
Теплота - это энергия, передаваемая от одной молекулы к другой в процессе нагревания или охлаждения вещества. Изменение теплоты влияет на скорость движения молекул и на силу притяжения между ними, что в свою очередь определяет состояние вещества.
Переход - это изменение состояния вещества при изменении условий, таких как температура или давление. Например, при нагревании твердого вещества до определенной температуры оно начинает плавиться и переходит в жидкое состояние.
Изучая эти понятия, мы сможем лучше понять, как и почему вещества находятся в различных состояниях и как они могут переходить из одного состояния в другое.
Физические состояния: твёрдое, жидкое, газообразное

Твёрдое состояние – это одно из основных состояний вещества, в котором оно обладает определенной формой и объемом. Молекулы или атомы в твёрдом состоянии тесно уплотнены и не имеют возможности свободно перемещаться. Это состояние обычно характеризуется жесткостью, прочностью и неизменностью формы вещества при воздействии внешних сил.
Жидкое состояние – другое распространенное состояние вещества, в котором оно обладает определенным объемом, но не имеет фиксированной формы. Молекулы или атомы в жидком состоянии свободно двигаются друг относительно друга, но остаются достаточно близко друг к другу. Жидкость обычно обладает текучестью и способностью заполнять любую емкость, принимая ее форму.
Газообразное состояние – самое подвижное и менее плотное состояние вещества, в котором оно не имеет определенной формы и объема. Молекулы или атомы в газообразном состоянии свободно и без ограничений перемещаются в пространстве. Газы обладают высокой подвижностью и могут с легкостью заполнять любое доступное пространство.
Изучение этих трех состояний вещества позволяет нам понять, как материя проявляет себя в различных условиях и объяснить множество физических явлений в нашем ежедневном опыте и в природе.
Взаимные превращения веществ: испарение, конденсация, плавление, кристаллизация, испарение

Когда мы рассматриваем вещество, мы можем заметить, что оно может находиться в разных состояниях. А что происходит, когда оно переходит из одного состояния в другое? В этом разделе мы поговорим о взаимных превращениях веществ и особенностях таких переходов.
Одним из способов перехода между состояниями является испарение. Здесь вещество преобразуется из жидкого состояния в газообразное. Вы, возможно, знаете это явление под именем "выкипание". Испарение происходит при достижении определенной температуры.
Другой интересный процесс - конденсация, при котором газообразное вещество превращается в жидкое состояние. Когда вы видите капли воды на поверхности, это и есть конденсация. Она происходит, когда газ охлаждается и теряет свою энергию, превращаясь в жидкость.
Третий процесс - плавление. Здесь твердое вещество переходит в жидкое состояние. Вспомните, как лед тает, превращаясь в воду. Это и есть плавление, которое происходит при определенной температуре, называемой температурой плавления.
Далее мы рассмотрим кристаллизацию, которая является обратным процессом плавления. Здесь жидкое вещество охлаждается и превращается в твердое состояние. Кристаллизация происходит при определенной температуре, называемой температурой кристаллизации.
И, наконец, мы вернемся к начальному процессу - испарению. Испарение - это процесс превращения жидкого вещества в газообразное. При достижении определенной температуры молекулы вещества получают достаточно энергии для выхода из жидкой среды и перехода в газообразное состояние.
Таким образом, мы рассмотрели различные переходы между состояниями вещества, такие как испарение, конденсация, плавление, кристаллизация и испарение. Каждый из этих процессов имеет свои особенности и происходит при определенных условиях, таких как температура или давление.
| Процесс | Пример |
|---|---|
| Испарение | Кипение воды |
| Конденсация | Пар на окне |
| Плавление | Таяние льда |
| Кристаллизация | Образование соли при охлаждении раствора |
| Испарение | Высыхание белья на солнце |
Молекулярное движение: особенности каждого формата
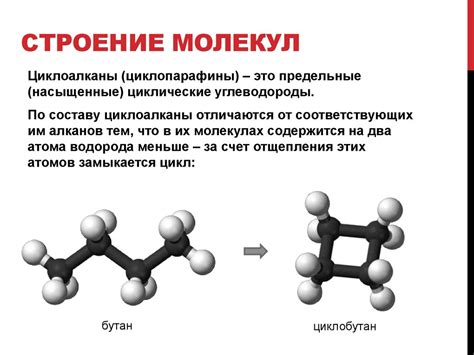
В твердом состоянии молекулы расположены вблизи друг от друга и выполняют колебания около равновесного положения. Их движение ограничено пространством и происходит с небольшой амплитудой. Молекулы взаимодействуют с соседними частицами через силы притяжения и отталкивания, что обеспечивает стабильность формы и объема твердого тела.
В жидком состоянии молекулы уже находятся на более больших расстояниях друг от друга, но все еще соседствуют. Их колебания становятся более свободными, с большей амплитудой. Молекулы жидкости способны перемещаться и менять свое положение относительно друг друга, поэтому они принимают форму сосуда или течут, не сохраняя фиксированную форму.
В газообразном состоянии молекулы движутся независимо друг от друга в разных направлениях с большой скоростью. Они находятся на больших расстояниях друг от друга и уже не взаимодействуют плотно. В газе молекулы могут быстро перемещаться, не препятствуя друг другу, и заполнять все доступное свободное пространство.
Таким образом, особенности молекулярного движения в каждом агрегатном состоянии отличаются друг от друга и влияют на свойства вещества, его форму, объем и способность к перемещению.
Твердые тела: уникальные свойства и внешний облик

Когда мы говорим о твердых телах, мы имеем в виду класс веществ, которые отличаются устойчивой формой и объемом, обладают фиксированной массой и не изменяют своих размеров при изменении условий окружающей среды. Эти характеристики и сочетание различных физических свойств делают твердые тела особенными и уникальными в мире веществ.
Свойства твердых тел:
- Непроницаемость: твердые тела обладают способностью препятствовать прохождению веществ через свою структуру. Именно благодаря этому свойству мы можем удерживать предметы и строить надежные конструкции.
- Разнообразие форм: твердые тела имеют различные геометрические формы, которые зафиксированы и не изменяются с течением времени без внешнего воздействия. Это позволяет создавать различные предметы и изделия с определенными функциональными свойствами.
- Прочность и твердость: твердые тела обладают высокой механической прочностью и твердостью, что позволяет им сопротивляться различным воздействиям и повреждениям. Именно благодаря этим свойствам строятся здания, мосты и другие инженерные сооружения.
- Теплопроводность: твердые тела хорошо проводят тепло, что позволяет им равномерно распределять тепловую энергию по своему объему. Это является важным свойством для различных приборов и механизмов, где требуется эффективное отвод тепла.
- Электропроводность: некоторые твердые тела обладают свойством проводить электрический ток. Это позволяет использовать эти вещества в электрических системах, проводниках и других устройствах.
Уникальность внешнего вида твердых тел и их характеристики делают их неотъемлемой частью нашей окружающей среды и позволяют создавать различные предметы, обладающие нужными свойствами и функциональностью.
Расположение атомов в твердом теле: регулярное и беспорядочное
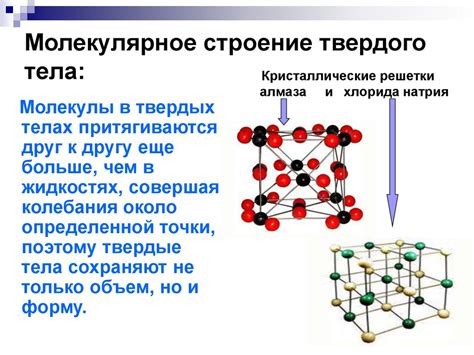
Когда мы говорим о твердом теле, мы обычно представляем себе прочную и прочную структуру, состоящую из атомов или молекул. Тем не менее, расположение этих атомов внутри твердого тела может быть очень разнообразным. И такое разнообразие расположения атомов сильно влияет на свойства твердого тела, такие как его прочность, плотность и электрическая проводимость.
Регулярное расположение атомов Регулярное расположение атомов означает, что атомы расположены в кристаллической решетке, которая имеет определенный и повторяющийся порядок. В кристаллической решетке каждый атом занимает свое строго определенное место и окружен другими атомами, которые также имеют строго определенное расположение. Примером регулярного расположения атомов может служить алмаз, где каждый углеродный атом связан с другими четырьмя атомами в форме тетраэдра. | Беспорядочное расположение атомов Беспорядочное расположение атомов означает, что атомы находятся в твердом теле без определенного порядка или структуры. В этом случае атомы могут находиться в положениях, которые не повторяются и не имеют определенного расположения относительно друг друга. Примером беспорядочного расположения атомов может служить стекло, которое обычно получается быстрым охлаждением расплавленного материала, при котором атомы не имеют времени установиться в кристаллической решетке. |
Изменение расположения атомов в твердом теле может изменить его свойства и может использоваться для создания материалов с уникальными характеристиками. Понимание регулярного и беспорядочного расположения атомов в твердом теле помогает ученым лучше осознавать принципы, лежащие в основе поведения и свойств твердых веществ и способствует разработке новых материалов с улучшенными свойствами.
Важные характеристики твердотельных материалов: проводимость электричества и тепла
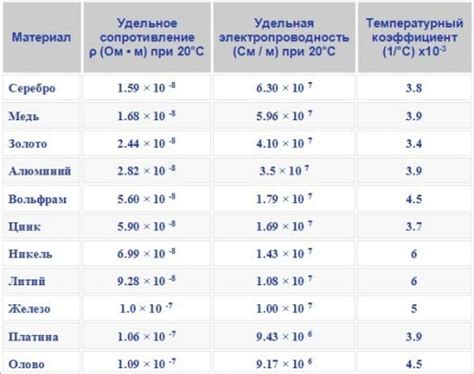
Проводимость электричества в твердотельных материалах - это способность материала пропускать электрический ток. Она определяется наличием или отсутствием свободных электронов, которые могут перемещаться внутри материала. Если твердотельное вещество содержит свободные электроны, то оно может быть проводником электричества. Например, металлы представляют собой твердотельные материалы с высокой проводимостью, так как их атомы имеют свободные электроны, способные перемещаться по всему объему материала.
Однако, не все твердотельные материалы обладают высокой проводимостью электричества. Например, диэлектрики, такие как стекло или резина, не имеют свободных электронов и, следовательно, не проводят электрический ток. Вместо этого, они обладают очень высоким сопротивлением электрическому току и могут быть использованы для изоляции проводов и электрических устройств.
Проводимость тепла в твердотельных материалах - это способность материала передавать тепловую энергию. Она зависит от физических свойств материала, таких как способность атомов или молекул передвигаться и взаимодействовать друг с другом. Некоторые твердотельные материалы, такие как металлы, обладают высокой проводимостью тепла, что делает их хорошими проводниками тепла. Они способны эффективно передавать тепло от одной точки к другой.
Однако, существуют и твердотельные материалы с низкой проводимостью тепла. Например, диэлектрики обладают низкой способностью передавать тепло и могут использоваться для теплоизоляции. Имея низкую проводимость тепла, они могут предотвращать передачу тепла через стены или изоляцию.
Жидкости: необычные свойства и взаимодействие молекул

В данном разделе мы рассмотрим жидкость как одно из агрегатных состояний вещества и обсудим особенности её свойств и взаимодействия молекул. Жидкость отличается от твёрдого и газообразного состояний не только своей формой, но и необычными свойствами, которые делают её особенной и интересной для исследования.
Свойства жидкостей
| Взаимодействие молекул в жидкостях
|
Вопрос-ответ

Что такое агрегатное состояние вещества?
Агрегатное состояние вещества - это форма, в которой находится вещество в зависимости от температуры и давления. Существуют три основных агрегатных состояния: твердое, жидкое и газообразное. В твердом состоянии молекулы вещества находятся на малых расстояниях друг от друга и имеют фиксированную форму и объем. В жидком состоянии молекулы уже находятся на больших расстояниях друг от друга и могут свободно перемещаться, при этом имея определенную форму, но не имея фиксированного объема. В газообразном состоянии расстояния между молекулами вещества велики, и они свободно перемещаются в пространстве, имея неопределенную форму и объем.
Какие особенности агрегатных состояний вещества?
Особенности агрегатных состояний вещества связаны с переходами между ними. Твердое вещество имеет определенную форму и объем, относительно неподвижные молекулы и обладает упругостью. Жидкое вещество может изменять свою форму, но имеет фиксированный объем, молекулы свободно перемещаются друг относительно друга, что позволяет им иметь свободную поверхность. Газообразное вещество не имеет фиксированной формы и объема, молекулы перемещаются случайно и заполняют имеющееся пространство.
Что происходит при изменении температуры агрегатных состояний вещества?
При изменении температуры агрегатные состояния вещества могут изменяться. Если температура твердого вещества повышается, то оно может перейти в жидкое состояние - это называется плавление. Если температура жидкого вещества уменьшается, то оно может перейти в твердое состояние - это называется затвердевание. При повышении температуры жидкости она может перейти в газообразное состояние - это называется испарение. В обратном случае, при снижении температуры газа, происходит конденсация - переход вещества из газообразного состояния в жидкое.
Что такое агрегатное состояние вещества?
Агрегатное состояние вещества - это способ, которым вещество существует и проявляет свои свойства при определенных условиях температуры и давления. В физике выделяют три основных агрегатных состояния: твердое, жидкое и газообразное.